
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1 mol·L-1的Na2CO3溶液:K+、Ba2+、NO3-、Cl-
B.0.1 mol·L-1FeCl3溶液:K+、NH4+、I-、OH-
C.8 mol·L-1HNO3的溶液:Fe2+、H+、Cl-、Na+
D.0.1 mol·L-1的NaOH溶液:K+、Na+、SO42-、CO32-
科目:高中化学 来源: 题型:
在105℃时1L两种气态混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积为10.5L,再将气体通过碱石灰,体积缩小6L。则下列各组混合烃中符合此条件的是( )
A.CH4,C4H8 B.CH4,C4H10 C.C2H4,C3H8 D.C2H2,C4H10
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省淄博市高二12月月考化学试卷(解析版) 题型:选择题
关于氯化铁水解的错误说法是
A.水解达到平衡(不饱和)时,无论加氯化铁饱和溶液还是加水稀释,平衡均向正方向移动
B.浓度为5mol/L和0.5mol/L的两种FeCl3溶液,其它条件相同时,Fe3+的水解程度前者比后者低
C.有50℃和20℃的相同浓度氯化铁溶液,其他条件相同时,Fe3+的水解程度前者比后者小
D.为抑制Fe3+水解,较好地保存FeCl3溶液,应加少量盐酸
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省淄博市高二12月月考化学试卷(解析版) 题型:选择题
在一定温度下,一定量的水中,石灰乳悬浊液存在下列平衡:
Ca(OH)2(s)  Ca2+(aq) + 20H-(aq),当向此悬浊液中加入少量氧化钙固体时,下列说法正确的是
Ca2+(aq) + 20H-(aq),当向此悬浊液中加入少量氧化钙固体时,下列说法正确的是
A.c(Ca2+)增大 B.c(Ca2+)不变
C.c(OH-)增大 D.Ca(OH)2固体的质量不变
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省东营市高一上学期第三次模块考试化学试卷(解析版) 题型:实验题
(8分)实验室用下列反应制取CO2和CO:H2C2O4 CO2 + CO + H2O,然后用下图所示装置将CO2和CO进行分离和干燥,已知分液漏斗中为稀硫酸,甲瓶中为NaOH溶液。试回答下列各题:
CO2 + CO + H2O,然后用下图所示装置将CO2和CO进行分离和干燥,已知分液漏斗中为稀硫酸,甲瓶中为NaOH溶液。试回答下列各题:
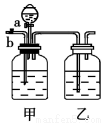
(1)乙瓶中装的是 ;
(2)关闭分液漏斗活塞a,打开b,通入混合气体,在右端收集到的气体是 ,甲中反应的离子方程式为 ;
(3)通入气体结束后,得到另一种气体的方法是:关闭活塞 (填写a或b,下空同)打开 ,在右端收集气体,此时甲中反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省东营市高一上学期第三次模块考试化学试卷(解析版) 题型:选择题
实验室可用如图所示的装置干燥、储存气体R,多余的气体可用水吸收,则R是

A.NO2 B.NO C.SO2 D.NH3
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省东营市高一上学期第三次模块考试化学试卷(解析版) 题型:选择题
下列物质中,不能由单质直接化合生成的是
①CuS ②FeS ③SO3 ④H2S ⑤FeCl2
A、①③⑤ B、①②③⑤ C、①②④⑤ D、全部
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邢台市高二12月月考化学试卷(解析版) 题型:选择题
离子晶体稳定性取决于晶体中晶格能的大小。判断KCl、NaCl、CaO、BaO四种晶体稳定性由高到低的顺序是
A.KCl>NaCl>BaO>CaO B.NaCl>KCl>CaO>BaO
C.CaO>BaO>NaCl>KCl D.CaO>BaO>KCl>NaCl
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市闵行区高二第一学期期末考试化学试卷(解析版) 题型:填空题
(本题共10分)
利用镁和稀硫酸反应,不仅可以测定1mol氢气的体积,装置如下左图,也可以测定镁带中镁的质量分数(杂质与酸反应不产生气体),装置如下右图。

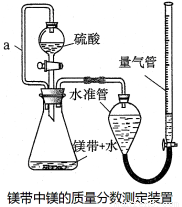
32.用离子方程式表示测定实验的反应原理 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com