
【题目】化学和环境保护、食品营养、材料应用等密切相关。
(1)防治环境污染,营造安全的生态环境已成为全人类的共识。
①天然水中杂质较多,常需加入明矾、氯化铁等作混凝剂进行处理,混凝剂溶于水后生成的胶体可以吸附水中的悬浮颗粒。请以明矾为例,用离子方程式表示该净水原理 。
②垃圾处理要遵循无害化、减量化和 的原则。
③在汽车尾气系统中装置催化转化器,由于含铅化合物会使 ,所以装有催化转化器的汽车必须使用无铅汽油。
(2)保证食品、药品安全,保持营养均衡,是人体健康的基础。
①人体需要的营养素主要有糖类、油脂、蛋白质、 、维生素和水。在氢、氮、铁、氯、钙这几种元素中,属于人体生命活动必需的微量元素是____________。
②抗酸药物的种类很多,其有效成分一般都是碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝和氢氧化镁等化学物质。某品牌抗酸药的主要成分有糖衣、碳酸镁、淀粉。
写出该抗酸药发挥功效时的离子方程式:__________________________。
③如果不注意控制酸性食物的摄入,就会导致血液偏酸,甚至形成“ 症”,引起人体缺钙、血液黏度增大等。
④阿司匹林是一种人工合成药物,结构简式如右图,常温下与NaOH反应可以得到可溶性钠盐,有比阿司匹林更好的疗效。 请写出此反应的方程式: 。
请写出此反应的方程式: 。
(3)丰富多彩的材料为人类的生存和发展创造了完美的物质条件。石英玻璃的主要成分为 。有机玻璃受热时会软化,易于加工成型。有机玻璃是一种 (选填“橡胶”或“纤维”或“塑料”)。有些塑料只是在制造过程中受热时能变软,可以塑制成一定的形状,但加工成型后就不会受热熔化,具有 。橡胶是制造轮胎的重要原料,天然橡胶通过硫化处理,使它的分子转化为________结构,从而增大橡胶的强度。
【答案】(1)①Al3++3H2O![]() Al(OH)3胶体+3H+ ②资源化 ③催化剂中毒
Al(OH)3胶体+3H+ ②资源化 ③催化剂中毒
(2)①无机盐 铁②MgCO3+2H+=Mg2++H2O+CO2↑ ③多酸
④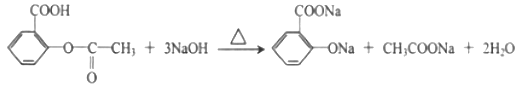
(3)SiO2 塑料 热固性 网状(体型)
【解析】
试题分析:(1)①明矾是KAl(SO4)212H2O,它能净水主要因为Al3+水解能生成Al(OH)3胶体:Al3+ + 3H2O ![]() Al(OH)3胶体 + 3H+。②垃圾处理要遵循无害化、减量化和资源化的原则。③在汽车尾气系统中装置催化转化器,由于含铅化合物会使催化剂中毒,所以装有催化转化器的汽车必须使用无铅汽油。
Al(OH)3胶体 + 3H+。②垃圾处理要遵循无害化、减量化和资源化的原则。③在汽车尾气系统中装置催化转化器,由于含铅化合物会使催化剂中毒,所以装有催化转化器的汽车必须使用无铅汽油。
(2)①人体需要的六大基本营养素主要有糖类、油脂、蛋白质、无机盐、维生素和水;铁、氯、钙这几种元素中,属于人体生命活动必需的微量元素是铁。
②糖衣、碳酸镁、淀粉中能与酸反应的是碳酸镁,它与酸反应生成二氧化碳和水:MgCO3+2H+=Mg2++H2O+CO2↑。
③如果不注意控制酸性食物的摄入,就会导致血液偏酸,甚至形成“多酸症”,引起人体缺钙、血液黏度增大等。
④此结构中的羧基和酯基都能与氢氧化钠反应所以反应方程式为:

(3)石英玻璃的主要成分为SiO2,有机玻璃是一种塑料,热固性是指塑料只是在制造过程中受热时能变软,可以塑制成一定的形状,但加工成型后就不会受热熔化;天然橡胶通过硫化处理,使它的分子转化为网状结构,从而增大橡胶的强度。


科目:高中化学 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法错误的是
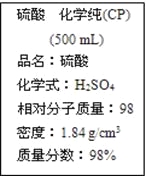
A. 该硫酸的物质的量浓度为18.4 mol/L
B. 该硫酸常用做干燥剂
C. 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL
D. 该硫酸与等质量的水混合后所得溶液的浓度大于9.2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
①碳元素参与生物体内所有化合物的组成
②地球上的生命是在碳元素的基础上建立起来的
③碳元素是各种大分子化合物中数量最多的元素
④碳元素是组成生物体内有机化合物的最基本元素
A. ②③④ B. ③④ C. ②④ D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学电池的说法中正确的是( )
A.化学电池只能将化学能转化为电能
B.燃料电池能将全部化学能转化为电能
C.锌银电池比能量大,电压稳定,储存时间长
D.一次电池包括干电池和蓄电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:“性最烈,能蚀五金……其水甚强,五金八石皆能穿第,惟玻璃可盛。”这里的“强水”是指( )
A.氨水 B. 硝酸 C.醋 D.卤水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为二氧化锰的有关转化关系图,有关说法中不正确的是

A.反应①~⑥均属于氧化还原反应
B.反应⑤中氧化剂与还原剂的物质的量之比为3∶4
C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶2
D.反应②中Cl2只作氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列配制的溶液浓度偏高的是
A. 配制稀盐酸用量筒量取浓盐酸时,俯视刻度线
B. 用量筒量取所需的浓盐酸倒入烧杯后,再用水洗量筒2-3次,洗液倒入烧杯中
C. 称量11.7 g NaCl配制0.2 mol/L NaCl溶液时,砝码错放在左盘
D. 定容时仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下图是某煤化工产业链的一部分,已知该产业链中某反应的平衡常数表达式为![]() ,已知此反应中生成1g氢气需吸热65.75kJ,它所对应的热化学方程式是 。
,已知此反应中生成1g氢气需吸热65.75kJ,它所对应的热化学方程式是 。

(2)向2L密闭容器中加入2molCO2、6molH2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)![]() CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)
①该反应自发进行的条件是 (填“低温”、“高温”或“任意温度”)
②下列叙述能说明容器内反应达到平衡状态的是 。
A.混合气体的平均相对分子质量保持不变 B.CO2和H2的体积分数保持不变
C.CO2和H2的转化率相等 D.混合气体的密度保持不变
(3)改变温度,使反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0中的所有物质都为气态,起始温度体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) △H<0中的所有物质都为气态,起始温度体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
反应I恒温恒容 | 0min | 2 | 6 | 0 | 0 |
10min | 4.5 | ||||
20min | 1 | ||||
30min | 1 | ||||
反应II绝热恒容 | 0min | 0 | 0 | 2 | 2 |
到平衡时,反应I、II对比,平衡时CH3OH的浓度c(I) c(II)(填“>”“<”或“=”)
反应I,前10min内的平均反应速率v(CH3OH)= 。若30min时只向容器中再充入1molCO2(g)和1molH2O(g),则平衡 移动。(填“正向”“逆向”或“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对实验过程的评价正确的是( )
A.某固体中加入稀盐酸,产生了无色气体,证明该固体一定是CaCO3
B.某溶液中滴加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含SO![]()
C.某无色溶液中滴入无色酚酞显红色,该溶液一定显碱性
D.验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加AgNO3溶液,有白色沉淀出现,证明含Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com