
用下列实验装置进行相应实验,能达到实验目的的是
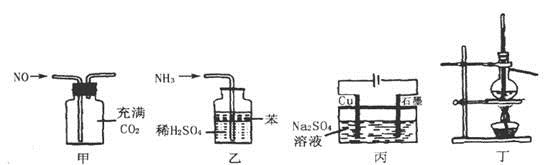
A. 用图甲所示装置(正放)可收集NO气体
B. 用图乙所示装置可吸收多余氨气且能防止倒吸
C. 用图丙所示装置可实现反应:Cu+2H2O Cu(OH)2+H2↑
Cu(OH)2+H2↑
D. 用图丁所示装置可分离乙醇(沸点78.3℃)与二甲醚(沸点24.9℃)的混合物
科目:高中化学 来源:2017届河北省高三上学期摸底考试化学试卷(解析版) 题型:选择题
下列反应中,反应后固体物质增重的是( )
A.氢气通过灼热的CuO粉末 B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热反应 D.将锌粒投入CuCl2溶液
查看答案和解析>>
科目:高中化学 来源:2017届河北省沧州市高三上周测化学试卷(解析版) 题型:选择题
已知溶液中:还原性HSO3―>I―,氧化性IO3―>I2>>SO32―。向含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如下图所示,下列说法正确的是

A.a点反应的还原剂是NaHSO3,被氧化的元素是碘元素
B.b点反应的离子方程式是:3HSO3-+IO3-+3OH-=3SO42-+I-+3H2O
C.c点到d点的反应中共转移0.6mol电子
D.往200ml 1mol/LKIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式是:
5HSO3-+2IO3-=I2+5SO42-+3H++H2O
查看答案和解析>>
科目:高中化学 来源:2017届河北省沧州市高三上周测化学试卷(解析版) 题型:选择题
常温下,1mol化学键分解成气态原子所需要的能量用E表示。根据表中信息判断下列说法不正确的是
共价键 | H—H | F—F | H—F | H—Cl | H—I |
E/(kJ·mol-1) | 436 | 157 | 568 | 432 | 298 |
A.432 kJ·mol-1>E(H—Br)>298 kJ·mol-1
B.表中最稳定的共价键是H—F键
C.H2(g)→2H(g) △H=+436 kJ·mol-1
D.H2(g)+F2(g)=2HF(g) △H=-25 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2017届河北省沧州市高三上周测化学试卷(解析版) 题型:选择题
下列化学反应的离子方程式表示正确的是
A.向Na2SiO3溶液中通入过量CO2:SiO32-+CO2+H2O=H2SiO3↓+CO32-
B.向Ca(HCO3)2溶液中滴加少量Ba(OH)2溶液:Ca2++2HCO3-+Ba2++2OH一=CaCO3↓+BaCO3↓+2H2O
C.向NaHSO4溶液中加入Ba(OH)2溶液至中性:H++SO42―+Ba2++OH―=BaSO4↓++H2O
D.Fe(OH)2沉淀中滴加稀硝酸:Fe(OH)2+2H+=Fe2++2H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高二下期末化学试卷(解析版) 题型:推断题
肉桂酸苄酯是一种重要的定香剂,可以由化合物A(C7H8O)和乙醛为原料来合成,其合成路线如下:
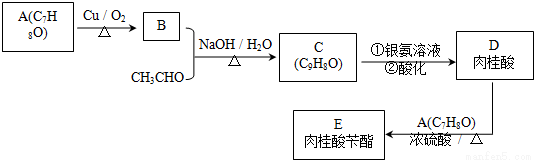
已知:①化合物A苯环上只有一个取代基,且能与钠反应生成氢气;
② 。
。
回答以下问题:
(1)B的化学名称是 ,C中所含的官能团的名称是 。
(2)写出D→E的反应类型 ,E的结构简式是 。
(3)写出A→B的化学方程式 。
(4)D可以形成一种高分子化合物F,F的结构简式是 。
(5)D的同分异构体有很多种,其中含有两个醛基且不能发生水解反应的同分异构体共有___________种。
(6)请按照上述线路,设计一条由CH3CH2OH为原料制备CH3CH2CH2CH2OH的合成线路,有机物用结构简式表示,无机试剂任选: 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上开学测化学试卷(解析版) 题型:填空题
下表为元素周期表的一部分。
| 碳 | 氮 | Y |
|
铝 | X |
| 硫 | Z |
请回答下列问题:
(1)Z元素在周期表中的位置为_______________。
(2)表中元素原子半径最大的非金属是(元素符号)_______________。
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是_______________;
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1 mol Y单质比1 mol S得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)碳与镁形成的1 mol 化合物Q与水反应,生成2 mol Mg(OH)2和1 mol烃,该烃分子中碳氢质量比为9:1。Q的化学式为_____________________。
(5)向氯化铝溶液中加入过量氨水,离子方程式为 。
(6)将SO2通入稀硝酸中,反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南师大附中高二上第一次月考化学卷(解析版) 题型:填空题
2013年雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)CO2是大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。目前,由CO2来合成二甲醚已取得了较大的进展,其化学反应是:
2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g) △H>0。
CH3OCH3(g) + 3H2O(g) △H>0。
①写出该反应的平衡常数表达式 。
②判断该反应在一定条件下,体积恒定的密闭容器中是否达到化学平衡状态的依据是 。
A.容器中密度不变
B.单位时间内消耗2molCO2,同时消耗1mol二甲醚
C.v(CO2)︰v(H2)=1︰3
D.容器内压强保持不变
(2)汽车尾气净化的主要原理为:2NO(g) + 2CO (g) 2CO2 (g) + N2 (g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:
2CO2 (g) + N2 (g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:
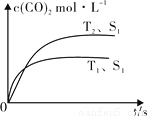
① 该反应的ΔH 0(选填“>”、“<”)。
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线。
(3)已知:CO(g) + 2H2(g) CH3OH(g)△H = ﹣a kJ•mol-1。
CH3OH(g)△H = ﹣a kJ•mol-1。
①经测定不同温度下该反应的平衡常数如下:
温度(℃) | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4 mol·L-1、c(H2)=0.4 mol·L-1、c(CH3OH)= 0.8 mol·L-1, 则此时v正 v逆(填“>”、“<”或“=”)。
0.8 mol·L-1, 则此时v正 v逆(填“>”、“<”或“=”)。
②某温度下,在体积固定的2L的密闭容器中将1 mol CO和2 mol H2混合,测得不同时刻的反应前后压强关系如下:
时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
则前15分钟,用氢气表示的平均化学反应速率为 ,达到平衡时CO的转化率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com