
【题目】下列过程属于物理变化的是
A. 煤的高温干馏
B. 汽车排气管上安装的催化转化器解决汽车尾气
C. 用金刚钻修补破损的瓷器
D. 自制“烤蓝”小刀
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:
【题目】海水晒盐的原理是( )
A.海水分解
B.温度升高,其他溶质的溶解度增大
C.升高温度,降低食盐在水中的溶解度
D.利用阳光、风力蒸发水分使氯化钠成晶体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于FeCl3溶液和Fe(OH)3胶体的说法中正确的是( )
A.都是无色透明、均一、稳定的分散系 B.分散质颗粒直径都在1~100 nm之间
C.Fe(OH)3胶体具有丁达尔效应 D.FeCl3溶液具有丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下将0.2 mol气体A充入10 L恒容密闭容器中,进行反应2A(g)+ B(g)![]() 2C(g)+D(s) △H<0,一段时间后反应达到平衡。此反应过程中测定的数据如下表所示,则下列说法正确的是( )
2C(g)+D(s) △H<0,一段时间后反应达到平衡。此反应过程中测定的数据如下表所示,则下列说法正确的是( )
t/min | 2 | 4 | 6 | 8 | 10 |
n(A)/mol | 0.16 | 0.13 | 0.11 | 0.10 | 0.10 |
A. 反应前2min的平均速率ν(C)=0.02mol·L-1·min-1
B. 平衡后降低温度,反应达到新平衡前ν(逆)> ν(正)
C. 其他条件不变,10min后再充入一定量的A,平衡正向移动,A的转化率变小
D. 保持其他条件不变,反应在恒压下进行,平衡时A的体积分数与恒容条件下反应相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是学生课外活动小组设计的制取氨气并进行氨气溶于水的喷泉实验等实验的装置示意图。
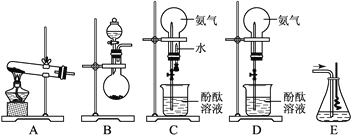
请回答下列问题:
(1)学生甲用图A所示装置制备氨气,写出该法制取氨气的化学方程式_________________;制出的氨气应使用________________法来收集,要得到干燥的氨气可选用____________做干燥剂。
(2)学生乙用图B所示装置也制出了氨气,他选用的制取试剂可能是__________和____________。
(3)学生丙用图C所示装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发水上喷的操作是____________________。
(4)学生丁将装置C误装为装置D,但经同学讨论后,认为也可引发喷泉。请说明用该装置引发喷泉的方法:___________________。
(5)学生戊用装置E(盛有水)吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入E装置的锥形瓶内,看到了具有催化作用的铂丝保持红热,同时瓶内生成了红棕色的气体。写出在此过程中可能发生反应的化学方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的用途是应用其化学性质的是( )
A.用铁罐储存浓硝酸
B.用MgO、Al2O3制作耐高温坩埚
C.用铁芯铝绞线作为高压输电线材料
D.用钠钾合金作为快中子反应堆的热交换剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M元素的1个原子失去2个电子转移到Y元素的2个原子中去,形成离子化合物Z.以下说法中错误的是( )
A.M形成+2价阳离子
B.Y形成+2价阳离子
C.Z可表示为MY2
D.Z的熔点较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)沉淀的生成、溶解和转化在无机物制备和提纯以及科研等领域有广泛应用。难溶物在水中溶解达到饱和时,即建立沉淀溶解平衡,平衡常数称为溶度积(Ksp)。已知25℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=1×10-9。
(1)将浓度均为0.1mol/L的BaCl2溶液与Na2SO4溶液等体积混合,充分搅拌后过滤,滤液中c(Ba2+)=________mol/L。取100mL滤液与100mL2mol/LNa2SO4的溶液混合,混合液中c(Ba2+)= ______mol/L。
(2)长期使用的锅炉需要定期除水垢,否则会降低燃料的利用率。水垢中含有的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去。
①CaSO4 转化为CaCO3的离子方程式为___________________
②请分析CaSO4 转化为CaCO3的原理____________________
(Ⅱ)联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为_________________。
(2)①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=________________,联氨和N2O4可作为火箭推进剂的主要原因为________________________。
(Ⅲ)某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。

(1)滴定
①用 _____式滴定管盛装0.1000 mol/L盐酸标准液,锥形瓶中装有25.00mL待测烧碱溶液。上图表示某次滴定时50 mL滴定管中前后液面的位置。请将用去的标准盐酸的体积填入②表空格中。
②有关数据记录如下:
滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
滴定前 | 滴定后 | 消耗的体积 | ||
1 | 25.00 | 0.50 | 25.95 | 25.45 |
2 | 25.00 | _______ | _______ | ______ |
3 | 25.00 | 6.00 | 31.55 | 25.55 |
(2)根据所给数据,计算出烧碱样品的物质的量浓度。c = _________________。
(3)对下列几种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
a.若滴定前用蒸馏水冲洗锥形瓶,则会使测定结果 ________ ;
b.读数时,若滴定前仰视,滴定后俯视,则会使测定结果__________ ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com