
对某酸性溶液(可能含有Br―,SO42—,H2SO3,NH4+)分别进行如下实验:①加热时放出的气体可以使品红溶液褪色;②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;③加入氯水时,溶液略显黄色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸。对于下列物质不能确认其在溶液中是否存在的是 ( )
A. Br― B. SO42— C. H2SO3 D. NH4+
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列叙述正确的是
A.目前使用的元素周期表中,最长的周期含有36种元素.
B.周期表中所有元素都是从自然界中发现的,过渡元素都是金属元素
C.非金属元素形成的共价化合物中,原子的最外层电子数只能是2或8
D.IA族与VIIA族元素间可形成共价化合物或离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
胶体区别于其它分散系的实质是( )
A.胶体可发生丁达尔效应 B.胶体粒子能够发生布朗运动
C.胶体能透过滤纸但不能透过滤纸 D.胶体粒子直径在1nm-100nm之间
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是某同学对NaHSO4的物质类型进行的分析,其中不正确的是( )
A.根据元素组成可判断是化合物
B.因它电离会生成钠离子又符合盐的组成,故可属于钠盐
C.因它电离会生成硫酸根离子又符合盐的组成,故可属于硫酸盐
D. NaHSO4溶于水可电离出氢离子故可以称为酸
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需要 0.1mol/L的 H2SO4溶液980mL,欲用 98%、密度为1.84g/cm3的浓硫酸配制.
(1)所需的主要仪器除量筒、烧杯、玻璃棒外,还需要 、 。
(2)其实验操作步骤可分为以下几步:
A.用量筒量取 mL浓硫酸,缓缓注入装有约50mL蒸馏水的烧杯里,并用玻璃棒搅拌。
B.用适量蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液都移入容量瓶里。
C.将稀释后的硫酸小心地用玻璃棒引流容量瓶里。
D.检查容量瓶是否漏水。
E.将蒸馏水直接加入容量瓶,至液面接近刻度线1-2cm处。
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液。
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻线相切。
请据此填写:
①完成上述步骤中的空白处。
②补充完成正确的操作顺序(用字母填写):
( D )→( A )→( C )→( )→( )→( )→( F )。
③将浓硫酸在烧杯中稀释后移入容量瓶时,必须_________________方可移液.
(3)试分析下列操作对所配溶液的浓度有何影响
①量取浓硫酸时眼睛俯视量筒刻度线,会导致所配溶液浓度会 ;(填: 偏高、偏低、或无影响,下同)
②定容时,眼睛仰视刻度线,所配溶液浓度会 ;
查看答案和解析>>
科目:高中化学 来源: 题型:
在化学学习中使用数轴的表示方法可收到直观、形象的效果,下列表达中正确的是( )
A.分散质微粒的大小与分散系种类的关系:
B.常温下溶液的pH其酸碱性的关系:
C.硫的化合物中化合价与其氧化性、还原性的关系: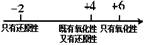
D.Fe在Cl2中燃烧的产物与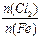 的关系:
的关系: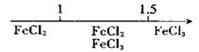
查看答案和解析>>
科目:高中化学 来源: 题型:
FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、NO的物质的量之比为1︰1︰1时,实际参加反应的FeS与HNO3的物质的量之比为( )
A.1∶6 B.1∶7 C.2∶11 D.16∶25
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度和压强下,1体积X2气体与3体积Y2气体化合生成2体积
某气体,则该气体的化学式为 ( )
A.XY3 B.XY C.X3Y D.X2Y3
查看答案和解析>>
科目:高中化学 来源: 题型:
以下有关元素性质的说法不正确的是
A.具有下列电子排布式的原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s222s2p63s23p4
原子半径最大的是①
B.具有下列价电子排布式的原子中,①3s23p1 ②3s23p2 ③3s23p3 ④3s23 p4 第一电离能最大是③
p4 第一电离能最大是③
C.①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的电负性随原子序数增大而递增的是④
D.某元素气态基态原子的逐级电离能分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com