
【题目】古代染坊常用某种“碱剂”精炼丝绸,该“碱剂”的主要成分是一种盐,能促进蚕丝表层丝胶蛋白杂质水解而除去,使丝绸颜色洁白、质感柔软、色泽光亮。这种“碱剂”可能是
A. 食盐 B. 烧碱 C. 草木灰 D. 明矾
科目:高中化学 来源: 题型:
【题目】研究含氮和含硫化合物的性质在工业生产和环境保护中有重要意义。
(1)制备硫酸可以有如下两种途径:
2SO2(g)+O2(g)=2SO3(g) △H=-198kJ·mol-1
SO2(g)+NO2(g)=SO3(g)+NO(g) △H=-41.8kJ·mol-1
若CO的燃烧热为283 kJ·mol-1,则1molNO2和1mol CO 反应生成CO2和NO的能量变化示意图中E2= _________kJ·mol-1

(2)锅炉烟道气含CO、SO2,可通过如下反应回收硫:2CO(g)+SO2(g)![]() S(I)+2CO2(g)。某温度下在2L恒容密闭容器中通入2 molSO2和一定量的CO发生反应,5min后达到平衡,生成1molCO2。其他条件不变时SO2的平衡转化率反应温度的变化如图A,请解释其原因:_________
S(I)+2CO2(g)。某温度下在2L恒容密闭容器中通入2 molSO2和一定量的CO发生反应,5min后达到平衡,生成1molCO2。其他条件不变时SO2的平衡转化率反应温度的变化如图A,请解释其原因:_________
②第8分钟时,保持其他条件不变,将容器体积迅速压缩至1L,在10分钟时达到平衡,CO的物质的量变化了1mol。请在图B中画出SO2浓度从6~11分钟的变化曲线。

(3)己知某温度下,H2SO3的电离常数为K1≈l.5×10-2, K2≈1.0×10-7,用NaOH溶液吸收SO2,当溶液中HSO3-, SO32-离子相等时,溶液的pH值约为_________
(4)连二亚硫酸钠(Na2S2O4)具有强还原性,废水处理时可在弱酸性条件下加入亚硫酸氢钠电解产生连二亚硫酸根,进而将废水中的HNO2还原成无害气体排放,连二亚硫酸根氧化为原料循环电解。产生连二亚硫酸根的电极反应式为_________,连二亚硫酸根与HNO2反应的离子方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列各组物质按单质、氧化物、酸、碱、盐分类顺序排列,其中正确的是
A. 银、干冰、硫酸、烧碱、纯碱
B. 碘酒、冰、盐酸、烧碱、食盐
C. 氢气、二氧化硫、硝酸、纯碱、硝酸钾
D. 铜、氧化铜、醋酸、石灰水、氯化铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过石油裂解可以获得乙烯,再以乙烯为原料还可以合成很多的化工产品,试根据下图回答有关问题:
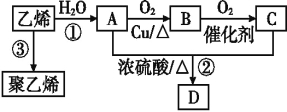
已知:有机物D是一种有水果香味的油状液体。
(1)有机物B的名称为 ,结构简式为 。
决定有机物A、C的化学特性的原子团的名称分别是 。
(2)写出图示反应②、③的化学方程式,并指明反应类型:
② ; 反应类型: 。
③ ; 反应类型: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率的说法中,正确的是
A. 2mol/L盐酸与锌反应时,加入4mol/L的氯化钠溶液,生成氢气的速率加快
B. 对于可逆反应2CO+2NO![]() N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快
N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快
C. 工业上合成氨是放热反应,升高温度,正反应速率减慢
D. 在K2SO4和BaCl2两溶液反应时,增大压强,生成沉淀速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2L的密闭容器通入两种气体后发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
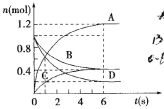
A.该反应的化学方程式为3B+4D=6A+2C
B.反应进行到6s时υ(B)=υ(C)
C.反应进行到6s时,用B表示的平均反应速率为0.05mol·L-1·s-1
D.反应进行到6s时,反应停止了
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】—定条件下,在恒容密闭容器中进行可逆反应:PCl5(g)![]() PCl3(g)+Cl2(g) △H>0,下列叙述不能说明反应已达到化学平衡状态的是
PCl3(g)+Cl2(g) △H>0,下列叙述不能说明反应已达到化学平衡状态的是
A. 容器压强保持不变
B. 混合气体的密度保持不变
C. 混合气体的平均相对分子质量不再改变
D. 相同时间内,生成1 mol PC15,同时生成1 mol PC13
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鉴别两种溶液食盐水和蔗糖水的方法有
①在两种溶液中分别加入少量稀硫酸,加热,再加入碱中和硫酸,再加入银氨溶液,微热;②测量溶液的导电性;③将溶液与溴水混合、振荡;④用舌头尝味道。
其中在实验室进行鉴别的正确方法是
A. ①② B. ①③ C. ②③ D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com