
对下列装置图的叙述正确的是
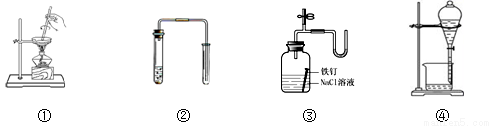
A.装置①可用于蒸发氯化镁溶液得到无水氯化镁
B.装置②可用于铜和稀硝酸制取并收集少量NO
C.装置③可用于证明铁生锈氧气参与反应
D.苯萃取碘水中的碘后,从装置④下口放出的是碘的苯溶液
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源:2015-2016学年江西省高一上第一次段考化学试卷(解析版) 题型:选择题
下列说法错误的是
A.从1L 1mol/L的氯化钠溶液中取出10ml,其浓度仍是1mol/L
B.制成0.5L 10mol/L的盐酸,需要氯化氢气体112L(标准状况)
C.10g 98%硫酸(密度为1.84g/cm3)与10mL18.4mol/L硫酸的浓度是不同的
D.0.5 L 2mol/L的氯化钡溶液中,钡离子和氯离子总数为3×6.02×1023
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省牡丹江市高三9月月考化学试卷(解析版) 题型:选择题
X、Y、Z、W为四种短周期主族元素。其中X、Z同主族,Y、Z同周期,W与X、Y既不同主族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是
A.X与W形成化合物稳定性一定强于Z与W形成化合物
B.Y、Z两元素的简单离子半径Y>Z
C.X、Y、Z对应气态氢化物的热稳定性和还原性强弱顺序一致
D.Y元素最高价氧化物对应水化物的化学 式为HYO4
式为HYO4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二9月月考化学试卷(解析版) 题型:填空题
依据事实,写出下列反应的热化学方程式。
(1)在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧热的热化学方程式为____________。
(2)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热为-57.3kJ/mol):_______。
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g) =N2O4 (1) △H1= -19.5kJ·mol-1
②N2H4 (1) + O2(g)=N2(g) + 2 H2O(g) △H2= -534.2kJ·mol-1
写出肼和N2O4 反应的热化学方程式_______。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省富阳市高三上学期第二次质量检测化学试卷(解析版) 题型:填空题
(10分)无机化合物A和金属B是中学化学常见的固体,其中A显淡黄色。相同质量的A、B都能与液体C反应放出气体,两气体又能恰好完全反应生成C。利用B在高温下的挥发性,可通过它的碳酸盐和焦炭在真空环境中来制备B。化合物D可作为有机反应中的脱氢试剂,1molD和1mol NH4Cl反应生成2mol气体E和1molB的氯化物。已知标准状况下气体E的密度为0.76g·L-1。
请回答下列问题:
(1)E的化学式为 。
(2)题中制备B的化学方程式为 。下列物质能替代焦炭的是 。
A.Na B.H2 C.KMnO4 D.Cl2
(3)B与E在一定条件下 (填“可能”或“不可能”)直接发生反应产生D,判断理由是 。
查看答案和解析>>
科目:高中化学 来源:2016届江西省九江市七校高三第一次联考化学试卷(解析版) 题型:选择题
X、Y、Z、W、Q都是短周期元素,其中X原子的最外层电子数是内层电子数的3倍;X与Z同族,Y与Z同周期,Q原子的电子总数等于其电子层数的3倍,W与X、Y既不同族也不同周期且W不为稀有气体元素;X、Y、Z三种元素的族序数之和为16。下列说法正确的是
A.Q与W能形成10电子, 不能形成14电子、18电子分子
B.Y的最高价氧化物对应水化物的化学式只能表示为H4YO4
C.Y、Z、Q分别与X化合,只能形成AB2型化合物
D.X、Z、W中的两种或三种元素形成的钠盐溶液可能显酸性、碱性、中性
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三第二次月考化学试卷(解析版) 题型:选择题
在含有FeCl3和BaCl2的酸性溶液中,通入足量的SO2后有白色沉淀生成,过滤后,向溶液中滴加KSCN溶液,无明显现象,下列叙述不正确的是
A.白色沉淀是BaSO4和BaSO3 B.溶液的酸性增强
C.白色沉淀是BaSO4 D.FeCl3全部被还原为FeCl2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二第一学期第一次月考化学试卷(解析版) 题型:填空题
(10分) (1)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的________腐蚀。为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,或与像铅酸蓄电池这样的直流电源的________极(填“正”或“负”)相连。
(2)基态Fe原子有 个未成对电子,Fe2+的电子排布式为 。可用铁氰化钾溶液检验 Fe2+,发生反应的离子方程式为 。
(3)用惰性电极电解200 mL一定浓度的硫酸铜溶液(不考虑电解过程中溶液体积变化),通电一段时间后,若向所得的溶液中加入0.1 mol Cu (OH)2,溶液恰好恢复到电解前的浓度和pH,则电解过程中转移电子的物质的量为________ mol。
(4)用铂作电极电解AlCl3溶液的总反应离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期二调化学试卷(解析版) 题型:选择题
下列说法中不正确的是
A.在燃煤中加入石灰石可减少SO2排放,发生的反应为2CaCO3 +2SO2 +O2 2CO2 +2CaSO4
2CO2 +2CaSO4
B.C02通入水玻璃可以得到硅酸沉淀
C.硅主要以单质、氧化物、硅酸盐的形式存在于自然界中
D.氢氟酸能够雕刻玻璃,故不能用玻璃瓶来盛装氢氟酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com