
| A. | 中性溶液中可能大量存在Fe3+、K+、Cl-、SO42- | |
| B. | 标准状况下,将1.12 L CO2气体通入1 L 0.1 mol/L的NaAlO2溶液中:CO2+2H2O+AlO2-═Al(OH)3↓+HCO3- | |
| C. | 由水电离出的c(H+)=1×10-12 mol/L 的溶液中可能大量存在K+、I-、Mg2+、NO3- | |
| D. | 向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═NH3•H2O+Al(OH)3↓+2BaSO4↓ |
分析 A.Fe3+在pH为4.4左右沉淀完;
B.n(CO2)=$\frac{1.12L}{22.4L/mol}$=0.05mol,n(NaAlO2)=0.1mol,二氧化碳不足,生成沉淀和碳酸钠;
C.由水电离出的c(H+)=1×10-12 mol/L 的溶液,为酸或碱溶液;
D.使SO42-完全沉淀,以1:2反应,生成硫酸钡、氢氧化铝和水.
解答 解:A.Fe3+在pH为4.4左右沉淀完,则中性溶液中不能大量存在Fe3+,故A错误;
B.n(CO2)=$\frac{1.12L}{22.4L/mol}$=0.05mol,n(NaAlO2)=0.1mol,二氧化碳不足,生成沉淀和碳酸钠,离子反应为CO2+3H2O+2AlO2-═2Al(OH)3↓+CO32-,故B错误;
C.由水电离出的c(H+)=1×10-12 mol/L 的溶液,为酸或碱溶液,碱溶液中不能大量存在Mg2+,酸溶液中I-、H+、NO3-发生氧化还原反应不能共存,故C错误;
D.使SO42-完全沉淀,以1:2反应,生成硫酸钡、氢氧化铝和水,离子反应为NH4++Al3++2SO42-+2Ba2++4OH-═NH3•H2O+Al(OH)3↓+2BaSO4↓,故D正确;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.


 特高级教师点拨系列答案
特高级教师点拨系列答案 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:填空题
 在如图所示的物质转化关系中(部分反应条件及产物省略),化合物A由短周期元素组成,所含离子数目比为1:2;B是常见的无色液体,C是能使湿润的红色石蕊试纸变蓝色的气体,E是淡黄色粉末,D、F、G均为无色气体.
在如图所示的物质转化关系中(部分反应条件及产物省略),化合物A由短周期元素组成,所含离子数目比为1:2;B是常见的无色液体,C是能使湿润的红色石蕊试纸变蓝色的气体,E是淡黄色粉末,D、F、G均为无色气体.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
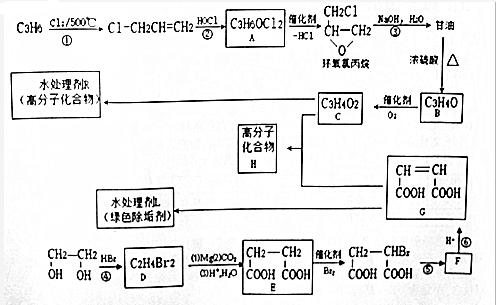
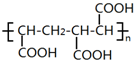 .
.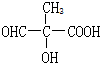 .
.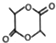 的合成路线(无机原料任选).(合成路线的常用表示方法为:A$→_{反应条件}^{反应试剂}$B$→_{反应条件}^{反应试剂}$目标产物).
的合成路线(无机原料任选).(合成路线的常用表示方法为:A$→_{反应条件}^{反应试剂}$B$→_{反应条件}^{反应试剂}$目标产物).查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 可以表示:Ca(HCO3)2溶液与Ca(OH)2溶液的反应 | |
| B. | 不能表示:Ca(HCO3)2溶液与Ba(OH)2溶液反应 | |
| C. | 可以表示:Ca(HCO3)2溶液与NaOH溶液反应 | |
| D. | 不能表示:NaHCO3溶液与Ca(OH)2溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

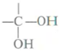 $\stackrel{自动脱水}{→}$
$\stackrel{自动脱水}{→}$
 .
.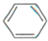 +
+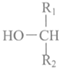 $\stackrel{酶}{→}$
$\stackrel{酶}{→}$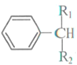 +H2O则可推知反应②发生时,会得到一种副产物,写出该副产物的结构简式
+H2O则可推知反应②发生时,会得到一种副产物,写出该副产物的结构简式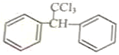 .
.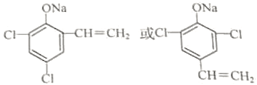 (任写一种)
(任写一种)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||
| Y | Z | W |
| T |
| A. | X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增 | |
| B. | Y、Z、X元素在自然界中均不能以游离态存在,它们氧化物对应水化物的酸性依次递增 | |
| C. | 根据元素周期律推测,金属性T比Y强 | |
| D. | W、Z的最高价对应的氧化物熔化时破坏的作用力相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在10g质量分数为46%的乙醇水溶液中含有H原子数目为1.2NA | |
| B. | 标准状况下22.4LNO与11.2LO2混合后气体的分子数为2NA | |
| C. | 4.0gH2与足量O2完全反应生成水,反应中断裂共价键数目为2NA | |
| D. | 常温常压下,将0.1molFe投入足量浓硝酸中,转移电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有机物 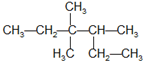 的系统命名为3,3-二甲基-2-乙基戊烷 的系统命名为3,3-二甲基-2-乙基戊烷 | |
| B. | 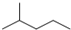 的一氯取代物的同分异构体有6种 的一氯取代物的同分异构体有6种 | |
| C. | 在相同条件下,等物质的量的乙烯和乙醇完全燃烧消耗的氧气体积相等 | |
| D. | 蔗糖、淀粉、纤维素、聚乙烯都属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com