
分析 同周期自左而右电负性增大,同主族自上而下电负性减小;p轨道最多排6个电子,如果p轨道半满,则p轨道排列3个电子,为第VA族元素;同周期自左而右金属性减弱,同主族元素从上到下,元素的金属性逐渐增强;同周期自左而右非金属性增强,同主族元素从上到下,元素的非金属性逐渐减弱,同一周期,元素的电负性随着原子序数的增大而增大,第二周期第ⅥA主族元素为氧元素,据此书写核外的电子排布式.
解答 解:同周期从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,故电负性最大的元素是F,最小的是第IA族的Cs,p轨道最多排6个电子,如果p轨道半满,则p轨道排列3个电子,为第VA族元素,第二周期为氮元素,第三周期为磷元素,第四周期为砷元素,同周期自左而右金属性减弱,同主族元素从上到下,元素的金属性逐渐增强,所以第IA元素中Cs最活泼,同周期自左而右非金属性增强,同主族元素从上到下,元素的非金属性逐渐减弱,所以最活泼的非金属元素是第ⅥIA元素中F,同一周期元素的第一电离能随着原子序数的增大而呈增大的趋势,所以第三周期第一电离能最小的元素是钠,最大的元素是Ar,第二周期第ⅥA主族元素为氧元素,氧元素为8号元素,原子核外有8个电子,其电子排布式为:1s22s22P4;
故答案为:F;Cs;N、P、As;Cs;F;Na;Ar;1S22S22P4.
点评 本题考查元素周期律和元素周期表、核外电子排布等,注意对基础知识的理解掌握,注意常考的考点电负性、电离能、金属性、非金属性等高频考点,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 乙酸乙酯和水,酒精和水,苯酚和水 | |
| B. | 二溴乙烷和水,溴苯和水,硝基苯和水 | |
| C. | 甘油和水,乙醛和水,乙酸和乙醇 | |
| D. | 油酸和水,甲苯和水,己烷和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
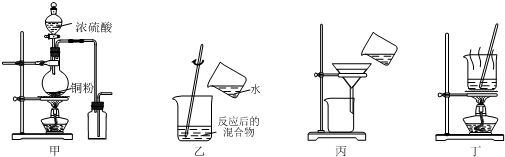
| A. | 用图甲装置制取并收集二氧化硫 | |
| B. | 用图乙装置向反应后的混合物中加水稀释 | |
| C. | 用图丙装置过滤出稀释后混合物中的不溶物 | |
| D. | 用图丁装置将硫酸铜溶液蒸发浓缩后冷却结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过渡元素包括七个副族和第Ⅷ族的元素 | |
| B. | 第3列中元素种类最多 | |
| C. | 第17列的第一种元素对应最高价氧化物的水化物是最强的含氧酸 | |
| D. | 第15列元素的氢化物组成通式可用RH3表示 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素、蛋白质都是天然高分子化合物 | |
| B. | 用于奥运“祥云”火炬的丙烷是一种清洁燃料 | |
| C. | 医疗上使用75%的酒精用于消毒 | |
| D. | 糖类、油脂、蛋白质在一定条件下都可发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 8:1 | C. | 1:1 | D. | 80:108 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数X>Y>Z | |
| B. | 元素的非金属性由强至弱的顺序是X>Y>Z | |
| C. | 原子半径大小顺序是X>Y>Z | |
| D. | 气态氢化物的稳定性H3X>H2Y>HZ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
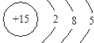 、其最高价氧化物对应的水化物的化学式H3PO4.
、其最高价氧化物对应的水化物的化学式H3PO4.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com