

| 0.15mol/L |
| 0.45mol/L |
| c2(NH3) |
| c(N2)c3(H2) |
| 0.12 |
| 0.1×0.33 |
| △c |
| △t |
| 0.003mol/L |
| 2L |


 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源:不详 题型:填空题
 O2 + Hb·CO,实验表明,Hb·CO的浓度即使只有Hb·O2的2℅,也足以使人的智力受损。试回答:(1)上述反应的平衡常数表达式为:K=_________________。(2)抽烟后,吸入肺部的空气中测得的CO和O2的浓度分别为10-6mol /L和10-2mol /L。已知37℃时,平衡常数K=220,这时Hb·CO的浓度________(填“大于”、“小于”或“等于”) Hb·O2浓度的0.02倍。
O2 + Hb·CO,实验表明,Hb·CO的浓度即使只有Hb·O2的2℅,也足以使人的智力受损。试回答:(1)上述反应的平衡常数表达式为:K=_________________。(2)抽烟后,吸入肺部的空气中测得的CO和O2的浓度分别为10-6mol /L和10-2mol /L。已知37℃时,平衡常数K=220,这时Hb·CO的浓度________(填“大于”、“小于”或“等于”) Hb·O2浓度的0.02倍。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 催化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
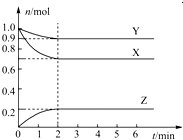
| A.用物质A表示的反应的平均速率为0.3mol?L-1?s-1 |
| B.用物质B表示的反应的平均速率为0.6mol?L-1?s-1 |
| C.2s时物质A的转化率为70% |
| D.2s时物质B的浓度为0.7mol?L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
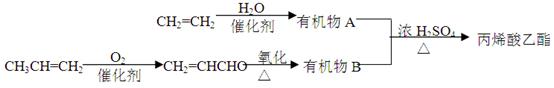
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HCHO溶液、(NH4)2SO4溶液均能使蛋白质变性 |
| B.煤的干馏是物理变化,煤的气化和液化是化学变化 |
| C.纤维素、蛋白质、油脂在一定条件下都能发生水解反应 |
| D.分子式为CH4O和C2H6O的物质一定互为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com