
【题目】X、Y、Z是三种原子序数依次递增的前10号元素,X的某种同位素不含中子,Y形成的单质在空气中体积分数最大,三种元素原子的最外层电子数之和为12,其对应的单质及化合物转化关系如图所示。下列说法正确的是______

A.原子半径:X<Z<Y,简单气态氢化物稳定性:Y<Z
B.A、C均为10电子分子,A的沸点高于C的沸点
C.E和F均属于离子化合物,二者组成中阴、阳离子数目之比均为1∶1
D.同温同压时,B与D体积比≤1∶1的尾气,可以用NaOH溶液完全处理
【答案】![]()
【解析】
由题意可知X为氢元素,Y为氮元素,Z为氧元素。则转化关系中的X2为H2,Y2为N2,Z2为O2,A为NH3,B为NO,C为H2O,D为NO2,E为HNO3,F为NH4NO3。原子半径:H<O<N,简单气态氢化物稳定性:NH3<H2O,A正确;NH3和H2O均为10电子分子,常温下NH3为气态,H2O为液态,沸点:NH3<H2O,B错误;HNO3属于共价化合物,不含阴、阳离子,NH4NO3属于离子化合物,阴、阳离子数目之比为1∶1,C错误;根据2NO2+2OH![]()
![]() +
+![]() +H2O,NO+NO2+2OH
+H2O,NO+NO2+2OH![]() 2
2![]() +H2O,所以,NO与NO2体积比≤1∶1的尾气,可以用NaOH溶液完全处理,D正确。
+H2O,所以,NO与NO2体积比≤1∶1的尾气,可以用NaOH溶液完全处理,D正确。


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
【题目】香豆素类化合物M具有抗病毒、抗癌等多种生物活性。下图是M和聚合物E的合成路线。
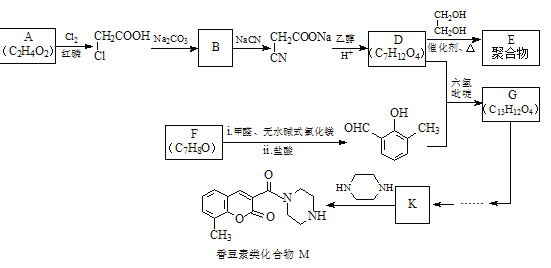
已知:
① ![]()
② ![]()
③ 
(1)A中官能团是_______。
(2)B→![]() 的反应类型是________。
的反应类型是________。
(3)化合物F能与FeCl3溶液发生显色反应,其结构简式是________。F有多种同分异构体,其中属于芳香族化合物、且为醇类物质的结构简式是________。
(4)G的结构简式是________。
(5)D→聚合物E的化学方程式是________。
(6)已知![]() ,将下列G→K的流程图补充完整:_____________________
,将下列G→K的流程图补充完整:_____________________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物E是一种除草剂,常通过如下方法合成:
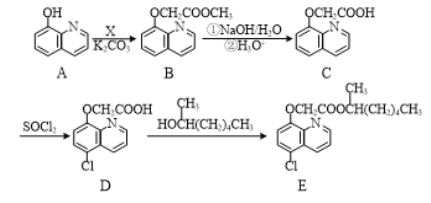
(1)化合物B中的含氧官能团的名称为酯基和_________。
(2)A与X发生反应生成B和HCl,则X的结构简式为_________________。
(3)D→E的反应类型为___________。
(4)写出同时满足下列条件的A的一种同分异构体的结构简式:_____________。
Ⅰ.分子中含有1个苯环,且有5个碳原子位于同一直线上。
Ⅱ.能与新制Cu(OH)2悬浊液反应。
Ⅲ.分子中含有4种化学环境不同的氢。
(5)已知:①CH3CHO![]() ClCH2CHO。②ClCH2CHO也能发生X在流程A→B中的类似反应。
ClCH2CHO。②ClCH2CHO也能发生X在流程A→B中的类似反应。
写出以苯酚和乙醛为原料合成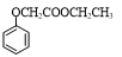 的合成路线流程图(无机试剂可任选)_______________。合成路线流程图示例如下:H2C=CH2
的合成路线流程图(无机试剂可任选)_______________。合成路线流程图示例如下:H2C=CH2![]() CH3CH2Br
CH3CH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以有机物A为原料通过一步反应即可制得重要有机化工产品P(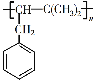 )。下列说法错误的是
)。下列说法错误的是
A.A的分子式为C11H14,可发生取代、氧化、加成等反应
B.由A生成P的反应类型为加成聚合反应,反应过程没有小分子生成
C.A的结构简式为![]() ,分子中所有碳原子不可能共面
,分子中所有碳原子不可能共面
D.1 mol A最多能与4 mol H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验操作和实验现象所得出的结论,正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向亚硫酸钠试样中滴入盐酸酸化的Ba(NO3)2溶液 | 产生白色沉淀 | 试样已经氧化变质 |
B | 乙醇和浓硫酸混合加热至170℃,将产生气体通入酸性KMnO4溶液 | 紫红色褪去 | 使溶液褪色的是乙烯 |
C | 在酒精灯上加热铝箔 | 铝箔熔化但不滴落 | 熔点:氧化铝>铝 |
D | 将炽热的木炭与浓硝酸混合所得气体通入澄清石灰水中 | 澄清石灰水不变浑浊 | 验证碳的氧化产物为CO |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO![]() +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
实验序号 | A溶液 | B溶液 |
① | 20mL0.1mol·L-1H2C2O4溶液 | 30mL0.1mol·L-1KMnO4溶液 |
② | 20mL0.2mol·L-1H2C2O4溶液 | 30mL0.1mol·L-1KMnO4溶液 |
(1)该实验探究的是___因素对化学反应速率的影响。如图一,相同时间内针筒中所得的CO2体积大小关系是___(填实验序号)。

(2)若实验①在2min末收集了2.24mLCO2(标准状况下),则在2min末,c(MnO![]() )=___mol·L-1(假设混合液体积为50mL)。
)=___mol·L-1(假设混合液体积为50mL)。
(3)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定___来比较化学反应速率。
(4)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是:①产物MnSO4是该反应的催化剂、②___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)下列物质中属于天然有机高分子化合物的是(填序号)____________________
①淀粉 ②油脂 ③高级脂肪酸 ④纤维素 ⑤蚕丝 ⑥聚乙烯塑料 ⑦涤纶
(2)写出该有机物![]() 的结构简式______________________________________它所属的类别为____________________(填序号)
的结构简式______________________________________它所属的类别为____________________(填序号)
①卤代烃 ②脂肪族化合物 ③脂环化合物 ④烯烃 ⑤烃的衍生物
(3)0.lmol某烃在足量的O2中燃烧,生成13.2gCO2和5.4gH2O,该烃的分子式为_______
(4)写出丙烯发生加聚反应的化学方程式_________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在体积为2 L的密闭容器中混合,并在一定条件下发生反应:2A(g)+B(g) ![]() xC(g),若经2 s后测得A的物质的量为2.8 mol,C的物质的量浓度为0.6 mol/L。现有下列几种说法:
xC(g),若经2 s后测得A的物质的量为2.8 mol,C的物质的量浓度为0.6 mol/L。现有下列几种说法:
①2 s内用物质A表示的平均反应速率为0.3 mol/(L·s);
②2 s内用物质B表示的平均反应速率为0.15 mol/(L·min)
③2 s时物质B的转化率为70%;
④x=2。
其中正确的是:
A. ①④ B. ②③ C. ①②③ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片。请回答下列问题:
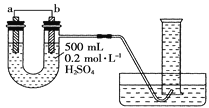
(1)b电极反应式为___。
(2)当量筒中收集到672mL(标准状况下)气体时,通过导线的电子的物质的量为__,此时a电极质量减少____g。
(3)如果将a、b两电极的电极材料对调,U形管中将出现的现象是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com