
| A. | 自然界中氢元素有三种同位素,它们的性质相同 | |
| B. | 三种同位素在化学反应中容易失去一个电子而呈+1价 | |
| C. | ${\;}_{1}^{1}$H原子失去一个电子后变成一个质子 | |
| D. | 氢在周期表中与碱金属同属ⅠA族 |
 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:解答题
| 元素 | X | Y | Z | W | R |
| 相 关 信 息 | 能形成+7价的化合物 | 日常生活中常见的金属,熔化时并不滴落,好像有一层膜兜着 | 通常状况下能形成短周期中最稳定的双原子分子,它是空气的主要成分之一 | 焰色反应为黄色 | 位于第ⅣA族,是形成化合物种类最多的元素 |


查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 装置中铜是负极 | |
| B. | 铜表面的反应为:2H++2e-=H2↑ | |
| C. | 电流的方向是从铁经导线流向铜 | |
| D. | 构成原电池后,铁与硫酸铜的反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 .下列有关双酚A的叙述不正确的是( )
.下列有关双酚A的叙述不正确的是( )| A. | 能和NaOH溶液反应 | B. | 能和FeCl3溶液发生显色反应 | ||
| C. | 能和浓溴水反应 | D. | 苯环上一溴代物有四种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
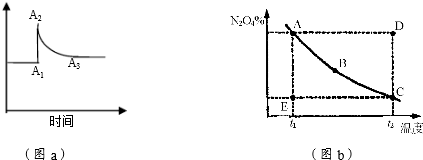
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 含苯酚的工业废水的处理流程如图所示.
含苯酚的工业废水的处理流程如图所示. ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4、NH3、HF | B. | OH-、F-、NH3 | C. | H3O+、NH4+、Mg2+ | D. | O2-、OH-、NH2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从氟到碘,其氢化物的稳定性逐渐减弱 | |
| B. | 因为铝原子比钠原子失去电子数目多,所以铝比钠的还原性强 | |
| C. | 第三周期从钠到氯,最高价氧化物的水化物碱性逐渐减弱,酸性逐渐增强 | |
| D. | 氧与硫为同主族元素,氧比硫的原子半径小,氧比硫的非金属性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 正极反应为Zn-2e-═Zn2+ | B. | 电池反应为Zn2++Cu═Zn+Cu2+ | ||
| C. | 在外电路中,电子从负极流向正极 | D. | 盐桥中的K+移向ZnSO溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com