
分析 (1)分子晶体熔化时破坏分子间作用力;原子晶体熔化破坏共价键;熔点的一般规律:原子晶体>离子晶体>分子晶体;
(2)含有离子键的化合物属于离子晶体;分子间通过分子间作用力结合形成的晶体属于分子晶体;原子间通过共价键形成的空间网状结构的晶体属于原子晶体.
解答 解:(1)分子晶体熔化时破坏分子间作用力,所以熔化时不需要破坏化学键的是干冰和碘片;原子晶体熔化破坏共价键,则熔化破坏共价键的是金刚石和SiO2;熔点的一般规律:原子晶体>离子晶体>分子晶体,原子晶体的熔点最高,由于金刚石中C-C键的键能大于SiO2中Si-O键的键能,所以金刚石的熔点高于二氧化硅,所以金刚石的熔点最高,干冰常温下为气体,所以熔点最低的是干冰;
故答案为:②;⑤;
(2)含有离子键的化合物属于离子晶体,所以BaCl2、NH4Cl、Na2SO4属于离子晶体;分子间通过分子间作用力结合形成的晶体属于分子晶体,所以属于分子晶体的是干冰和碘片;原子间通过共价键形成的空间网状结构的晶体属于原子晶体,所以属于原子晶体的是金刚石;
故答案为:①③④,⑤⑥,②.
点评 本题考查的知识点较多,侧重考查学生对离子键、共价键、晶体类型的判断和熔点的比较等知识点,注意把握离子晶体、分子晶体、原子晶体的辨别.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
 如图表示前36号元素的原子序数和气态原子失去核外第一个电子所需的能量(eV)的变化关系,其中A、B、C各点表示的元素是( )
如图表示前36号元素的原子序数和气态原子失去核外第一个电子所需的能量(eV)的变化关系,其中A、B、C各点表示的元素是( )| A. | N、S、P | B. | F、Cl、O | C. | He、Ne、Ar | D. | Si、C、B |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 反应类型取代反应.
反应类型取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
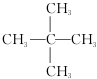 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
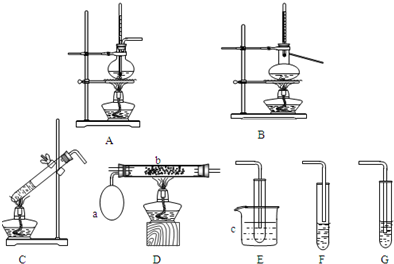
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
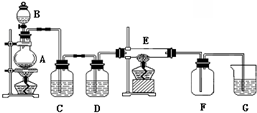
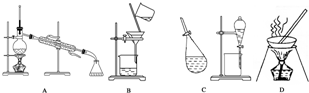
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③⑤ | C. | ①③④ | D. | ①④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com