
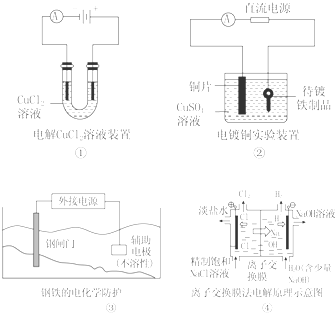
| A. | ①中阴极处能产生使湿润淀粉KI试纸变蓝的气体 | |
| B. | ②中待镀铁制品应与电源正极相连 | |
| C. | ③中钢闸门应与外接电源的正极相连 | |
| D. | ④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
分析 A、①装置是电解池,阴极是阳离子得到电子发生还原反应;
B、②装置待镀制品和电源负极相连做电解池的阴极;
C、③装置是电解池,在电解池中,阴极被保护;
D、④装置离子交换膜允许离子通过,氯气不能通过.
解答 解:A、①装置是电解池,阴极是溶液中阳离子得到电子发生还原反应,应是铜离子得到电子生成铜,故A错误;
B、②装置中待镀制品上要有Cu2+放电析出铜,故应和电源负极相连做电解池的阴极,故B错误;
C、③装置是电解池,在电解池中,阴极被保护,故钢闸门应与外接电源的负极相连,故C错误;
D、氯气是酸性气体,能和氢氧化钠反应.而氯气在阳极生成,NaOH在阴极生成,而④装置中的离子交换膜允许离子通过,氯气不能通过,可以避免生成的Cl2与NaOH溶液反应,故D正确;
故选D.
点评 本题考查了电解池、原电池工作原理的应用,电极名称、电极判断、电极反应、电子流向、电解应用等基础知识,熟练掌握基础是解题关键.


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:多选题
| A. | c(NH4+)相等的(NH4)2SO4、(NH4)2Fe(SO4)2和NH4Cl溶液中,溶质浓度大小:c[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c(NH4Cl) | |
| B. | 室温下若0.3mol•L-1HY溶液与0.3mol•L-1NaOH溶液等体积混合后,溶液的pH=9,则c(OH-)-c(HY)=c(H+)=1×10-9mol•L-1 | |
| C. | 室温下0.2mol•L-1HCl溶液与等体积0.05mol•L-1Ba(OH)2溶液混合后,溶液的pH=1 | |
| D. | NaHCO3溶液中:c(OH-)═c(H+)+c(H2CO3)+c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 活化分子具有的能量就是活化能 | |
| B. | 增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增大 | |
| C. | 无论是吸热反应还是放热反应,升高温度都能增大活化分子百分数 | |
| D. | 活化分子间的碰撞一定是有效碰撞 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水只含有氯分子和次氯酸分子 | |
| B. | 新制氯水可使紫色石蕊试液先变红后褪色 | |
| C. | 氯水光照时有气泡逸出,该气体的主要成分是氯气 | |
| D. | 氯水放置数天后,其酸性逐渐减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 | |
| B. | 用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 | |
| C. | 用激光笔验证淀粉溶液的丁达尔现象 | |
| D. | 用洁净的玻璃棒蘸取碳酸钾溶液在酒精灯火焰上灼烧,可观察到明亮的紫色火焰 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
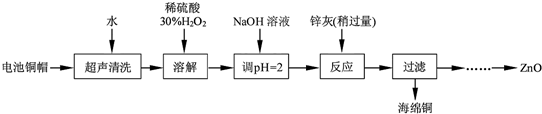
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
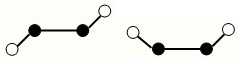
 ,有关该晶体的说法正确的是
,有关该晶体的说法正确的是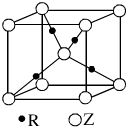
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com