
| A.稳定性H2S>HCl>HBr>HI |
| B.酸性HClO4>H2SO4>CH3COOH>H2CO3 |
| C.粒子半径S2-<Cl-<K+<Ca2+ |
| D.沸点HI>HBr>HCl>HF |
科目:高中化学 来源:不详 题型:问答题
| 实验方案 (只填写选用试剂序号) | 实验现象 | 结论 | |
| (1) | ______ | 一支试管中有白色沉淀生成,另一支试管中先生成白色沉淀,后白色沉淀消失 | 金属性:______ |
| (2) | ______ | ______ | 非金属性:Cl>Br |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素非金属性:F>O>N |
| B.热稳定性:PH3>H2S>HCl |
| C.酸性:HClO4>H3PO4>H2SO4 |
| D.原子半径:Al>Mg>Na |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Y、Z的气态氢化物,前者更稳定 |
| B.Z、W的最高价氧化物对应水化物的酸性,前者强 |
| C.X、W的气态氢化物相互反应,生成物中既含离子键又含共价键 |
| D.Y、W的单质,均可通过电解的方法获得 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.非金属性:Y>Z>M |
| B.M2是由非极性共价键构成的分子 |
| C.原子半径:M>Z>Y |
D.Y离子的结构示意图可表示为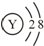 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.单质碲在常温下是固体 |
| B.H2TeO4的酸性比H2SO4的酸性弱 |
| C.H2Te不如HI稳定 |
| D.Te元素位于第六周期ⅥA族 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.第15列元素的最高价氧化物为R2O5 |
| B.第2列元素中肯定没有非金属元素 |
| C.L层电子数为偶数的所有主族元素所在族的族序数与元素原子L层电子数相等 |
| D.M层电子数为奇数的所有主族元素所在族的族序数与元素原子M层电子数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com