
| A、1 mol Cl2参加反应转移的电子数一定为2NA个 |
| B、CO2通过Na2O2使固体增重b g时,反应中转移的电子数为bNA/44个 |
| C、标准状况下,含NA个氩原子的氩气体积约为22.4 L |
| D、一定条件下,Al与Fe3O4反应,生成5.6 g Fe时,转移0.3NA个电子 |
| 8 |
| 3 |
| bg |
| 28g/mol |
| b |
| 28 |
| b |
| 28 |
| b |
| 28 |
| 1 |
| 2 |
| b |
| 56 |
| b |
| 28 |
| 8 |
| 3 |
| 8 |
| 3 |
| 4 |
| 15 |
| 4 |
| 15 |


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
| 化学键 | C-H | C-F | H-F | F-F |
| 键能 | 414 | 489 | 565 | 158 |
查看答案和解析>>
科目:高中化学 来源: 题型:
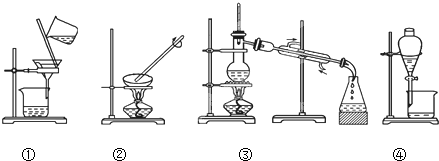
查看答案和解析>>
科目:高中化学 来源: 题型:
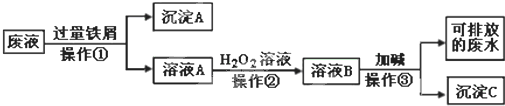
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、先加HCl,再加HBr |
| B、先加Cl2再加HBr |
| C、先加HCl,再加Br2 |
| D、先加HBr,再加HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
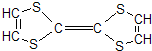 用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构如图所示.关于其性质的描述不正确的是( )
用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构如图所示.关于其性质的描述不正确的是( )| A、能使溴水和酸性KMnO4溶液褪色 |
| B、1mol该物质可与3molH2完全加成 |
| C、该物质在空气燃烧产生刺激性气体 |
| D、该物质属于烯烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ | ||
| B、AlCl3溶液中加入过量的浓氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ | ||
C、用小苏打治疗胃酸过多:CO
| ||
| D、用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2O+O2+4e-=4OH- |
| B、2H++2e-=H2↑ |
| C、Fe-2e-=Fe2+v |
| D、Fe-3e-=Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com