
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。请回答下列问题:
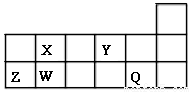
(1)W在周期表中的位置是___________,Y、Z的离子半径由大到小的顺序为___________ (用元素符号表示);由X与氢元素组成四原子化合物的电子式为__________。
(2)下列说法正确的是____________。
a.XY2和WY2都能溶于水生成对应的酸
b.Q的含氧酸的酸性比X的含氧酸的酸性强
c.X的最简单气态氢化物的稳定性大于W的最简单气态氢化物的稳定性
d.由NaOH溶液分别滴入MgQ2、ZQ3溶液中的反应现象可比较Mg和Z金属性的强弱
(3)自来水厂常用QY2对饮用水进行消毒,处理后的水中要求QY2的浓度在0.10~0.80 mg·L-1之间。碘量法可以检测水中QY2的浓度,步骤如下:
操作Ⅰ:取一定体积的水样,加入一定量的碘化钾,再用NaOH溶液调至中性,并加入淀粉溶液,溶液变蓝。
操作Ⅱ:再加入一定量的Na2S2O3溶液。(已知:2S2O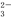 +I2=S4O
+I2=S4O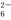 +2I-)
+2I-)
操作Ⅲ:然后再加硫酸调节水样pH至1~3。
操作时,不同pH环境中Q元素粒子种类及化合价如图所示:
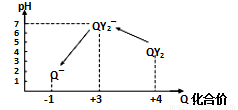
①操作Ⅰ中反应的离子方程式是_________________________。
②确定操作Ⅱ完全反应的现象是_________________________。
③在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是______________________。
④若水样的体积为1.0 L,在操作Ⅱ中消耗了1.0×10-3mol·L-1的Na2S2O3溶液10 mL,则水样中QY2的浓度是_______________mg·L-1(精确到0.01)。
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源:2016-2017学年广西省高一上模拟考试化学卷(解析版) 题型:选择题
某白色粉末由两种物质组成,为鉴别其成分进行如下实验:①取少量样品加入足量水仍有部分固体未溶解;再加入足量稀盐酸,有气泡产生,固体全部溶解;②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。该白色粉末可能为
A. NaHCO3、Al(OH)3 B. AgCl、NaHCO3 C. Na2SO3、BaCO3 D. Na2CO3、CuSO4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上模拟考试化学卷(解析版) 题型:选择题
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体
A. ①和② B. ①和③ C. ③和④ D. ①和④
查看答案和解析>>
科目:高中化学 来源:2017届四川省绵阳市高三第二次诊断性考试化学试卷(解析版) 题型:填空题
合成氨工业涉及固体燃料的气化,需要研究CO2与CO之间的转化。为了弄清其规律,让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g) 2CO(g) ∆H,测得压强、温度对CO、CO2的平衡组成的影响如图所示:
2CO(g) ∆H,测得压强、温度对CO、CO2的平衡组成的影响如图所示:
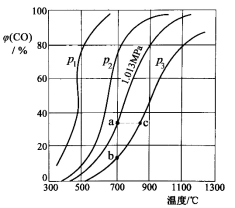
回答下列问题:
(1)p1、p2、p3的大小关系是______________,欲提高C与CO2反应中CO2的平衡转化率,应采取的措施为 。图中a、b、c三点对应的平衡常数大小关系是____________。
(2)900 ℃、1.013 MPa时,1 mol CO2与足量碳反应达平衡后容器的体积为V,CO2的转化率为_________,该反应的平衡常数K= 。
(3)将(2)中平衡体系温度降至640 ℃,压强降至0.1013 MPa,重新达到平衡后CO2的体积分数为50%。条件改变时,正反应和逆反应速率如何变化?____________,二者之间有何关系?___________。
(4)一定条件下,在CO2与足量碳反应所得平衡体系中加入H2和适当催化剂,有下列反应发生:
CO(g)+3H2(g) CH4(g)+H2O(g) ∆H1=-206.2 kJ/mol
CH4(g)+H2O(g) ∆H1=-206.2 kJ/mol
CO(g)+H2O(g) CO2(g)+H2(g) ∆H2=-41.2 kJ/mol
CO2(g)+H2(g) ∆H2=-41.2 kJ/mol
① 则二氧化碳与氢气反应转化为甲烷和水蒸气的热化学方程式是_________________。
② 已知298 K时相关化学键键能数据为:
化学键 | H—H | O—H | C—H |
|
E/(kJ·mol-1) | 436 | 465 | 413 | 1076 |
则根据键能计算,∆H1= ,它与上述实测值差异较大的原因可能是 。
查看答案和解析>>
科目:高中化学 来源:2017届四川省绵阳市高三第二次诊断性考试化学试卷(解析版) 题型:选择题
下列关于常见有机物的说法正确的是
A.乙醚和乙醇互为同分异构体
B.糖类、油脂、蛋白质均能发生水解反应
C.聚氯乙烯可用作生产食品包装材料的原料
D.分子式为C3H8O的有机物,只有2种能发生酯化反应
查看答案和解析>>
科目:高中化学 来源:2017届天津市五区县高三上学期期末考试化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.在常温下SiO2(s)+2C(s)=Si(s)+2CO(g)不能自发进行,则该反应的∆H>0
B.常温下,NH4Cl溶液加水稀释,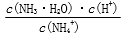 不变
不变
C.向硅酸钠溶液中滴加酚酞,溶液变红,证明Na2SiO3发生了水解
D.如图可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
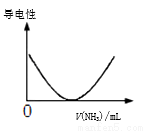
查看答案和解析>>
科目:高中化学 来源:2017届天津市五区县高三上学期期末考试化学试卷(解析版) 题型:选择题
根据下列实验现象或结果不能证明一元酸HR为弱酸的是
A.HR溶液中滴加紫色石蕊试液,溶液变红色
B.室温时,NaR溶液的pH大于7
C.HR溶液加入少量NaR固体,溶解后溶液的pH变大
D.室温时,0.01 mol·L-1的HR溶液pH=4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:实验题
以下是实验室对中草药中可能残余的有毒元素砷的检验步骤(As在中草药中主要以As2O3形式存在):
① 取1000g样品进行前期处理制得待测溶液,此时样品中可能含有的砷元素将转化为H3AsO3;
② 将待测溶液转移至250mL锥形瓶中,并滴入2~3滴0.2%的淀粉溶液;
③ 用浓度为1.5×10-3mol/L的标准碘溶液滴定待测溶液至终点,消耗20.25ml标准I2溶液,发生反应:H3AsO3+I2+H2O→H3AsO4+I-+H+(未配平):
(1)对少量中草药样品进行前期处理制得待测溶液的操作过程是:取少量样品于坩埚内灼烧成灰, 。
(2)配平:______H3AsO3+______I2 +______H2O = ______H3AsO4+_______I-+_______H+
(3)0.2%的淀粉溶液的作用是_______,如何判断滴定到达终点?________。
(4)实验室用一定量的KIO3和过量的KI以及酸混合反应制得的标准碘溶液,该反应的离子反应方程式为_____________________。
(5)我国药用标准限定:中药的砷含量不超过2.000mg/kg,通过计算可知,该样品砷含量约为_______mg/kg,故该草药样品________(“合格”或“不合格”)。(相对原子质量As-75)
查看答案和解析>>
科目:高中化学 来源:2016-2017黑龙江牡丹江第一高级中学高一上期末化学卷(解析版) 题型:选择题
下列各组物质中,Y是X物质中含有的少量杂质,Z是除杂试剂,其中所加试剂最合理的一组是( )
| X | Y | Z |
A | CO2 | SO2 | 饱和Na2CO3溶液 |
B | HCl | Cl2 | 饱和NaCl溶液 |
C | Fe2O3 | Al2O3 | NaOH溶液 |
D | Na2SO4溶液 | Na2CO3 | 盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com