
ЁОЬтФПЁПЯТСаЙигкгаЛњЮяЕФЫЕЗЈе§ШЗЕФга(ЁЁЁЁ)
ЂйБНЕФСкЮЛЖўТШШЁДњЮяжЛгавЛжж
ЂкМзЭщЕФЖўТШШЁДњВњЮягаСНжж
ЂлC3H8ЕФЖўТШДњЮяЙВга4жж
ЂмПЩгУЫсадИпУЬЫсМиШмвКГ§ШЅввЭщжаЕФввЯЉ
ЂнЗжзгЪНЪЧC4H8ЕФЬўЗжзгжавЛЖЈКЌгаЬМЬМЫЋМќ
ЂоНЋБНЕЮШыфхЫЎжа,еёЕДКѓЫЎВуНгНќЮоЩЋЪЧвђЮЊБНгыфхЫЎЗЂЩњСЫШЁДњЗДгІ
ЂпБНЕФЭЌЯЕЮяЪЧЗжзгжаНіКЌгавЛИіБНЛЗЕФЫљгаЬўРрЮяжЪ
ЂрЗЦЕФНсЙЙМђЪНЮЊ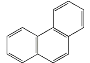 ,ЫќгыЯѕЫсЗДгІ,ПЩЩњГЩ5жжвЛЯѕЛљШЁДњЮя
,ЫќгыЯѕЫсЗДгІ,ПЩЩњГЩ5жжвЛЯѕЛљШЁДњЮя
A. 2ИіB. 3ИіC. 4ИіD. 5Иі
ЁОД№АИЁПB
ЁОНтЮіЁП
ЂйБНЕФСљИіЬМЬММќЭъШЋЯрЭЌЃЌЫЕУїБНЗжзгжаВЛКЌгаЕЅЫЋМќНЛЬцЃЌЙЪЂйе§ШЗЃЛ
ЂкМзЭщЕФЗжзгЙЙаЭЪЧе§ЫФУцЬхЃЌЦфжаCдзгЮЛгке§ЫФУцЬхЕФЬхаФЃЌHдзгЮЛгкЖЅЕуЃЌдђМзЭщЕФЖўТШШЁДњВњЮяжЛгавЛжжЃЌЙЪЂкДэЮѓЃЛ
Ђл C3H8ЕФЖўТШДњЮягаCH3CH2CHCl2ЁЂCH3CCl2CH3ЁЂCH2ClCH2CH2ClЁЂCH2ClCHClCH3 4жжЃЌЙЪЂле§ШЗЃЛ
ЂмЫсадИпУЬЫсМиШмвКНЋввЯЉбѕЛЏЩњГЩCO2ЃЌв§ШыСЫаТдгжЪЃЌЙЪЂмДэЮѓЃЛ
ЂнЗжзгЪНЪЧC4H8ЕФЬўЗжзгжаЃЌПЩФмЪЧЛЗЖЁЭщЃЌЛЗЖЁЭщВЛКЌгаЬМЬМЫЋМќЃЌЙЪЂнДэЮѓЃЛ
ЂоНЋБНЕЮШыфхЫЎжаЃЌеёЕДКѓЫЎВуНгНќЮоЩЋЪЧвђЮЊфхЫЎжаЕФфхЕЅжЪБЛБНнЭШЁЃЌВЂЮДЗЂЩњШЁДњЗДгІЃЌЙЪЂоДэЮѓЃЛ
ЂпБНЕФЭЌЯЕЮяЪЧжИ1ИіБНЛљгы1ИіЛђЖрИіЭщЛљЙЙГЩЕФЬўЃЌШєЭщЛљИФЮЊЯЉЬўЛљЁЂШВЬўЛљЛђЛЗЭщЬўЛљЃЌМДЪЙжЛКЌвЛИіБНЛЗЃЌвВВЛЪЧБНЕФЭЌЯЕЮяЃЌЙЪЂпДэЮѓЃЛ
ЂрЗЦЕФНсЙЙМђЪНЮЊ ЮЊЖдГЦНсЙЙЃЌвдащЯпЮЊЛљзМЖдГЦЃЌгаШчЭМЫљЪОЕФ5жжHдзг
ЮЊЖдГЦНсЙЙЃЌвдащЯпЮЊЛљзМЖдГЦЃЌгаШчЭМЫљЪОЕФ5жжHдзг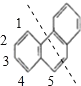 ЃЌЫљвдгыЯѕЫсЗДгІЃЌПЩЩњГЩ5жжвЛЯѕЛљШЁДњЮяЃЌЙЪЂре§ШЗЃЛ
ЃЌЫљвдгыЯѕЫсЗДгІЃЌПЩЩњГЩ5жжвЛЯѕЛљШЁДњЮяЃЌЙЪЂре§ШЗЃЛ
ЙЪбЁBЁЃ


 НнОЖбЕСЗМьВтОэЯЕСаД№АИ
НнОЖбЕСЗМьВтОэЯЕСаД№АИ аЁЗђзгШЋФмМьВтЯЕСаД№АИ
аЁЗђзгШЋФмМьВтЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЃКЂй 2C(s)+O2(g)=2CO(g)ЃЛІЄH= -220kJЁЄmol-1
Ђк ЧтЦјШМЩеЕФФмСПБфЛЏЪОвтЭМЃК
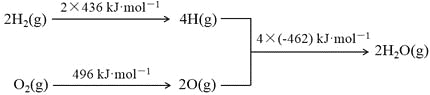
ЯТСаЫЕЗЈе§ШЗЕФЪЧ
A.1mol C(s)ЭъШЋШМЩеЗХГі110 kJЕФШШСП
B.H2(g)+1/2O2(g)=H2O(g)ЃЛІЄH= -480kJЁЄmol-1
C.C(s)+H2O(g)=CO(g)+H2(g)ЃЛІЄH= +130kJЁЄmol-1
D.гћЗжНт2mol H2O(l)ЃЌжСЩйашвЊЬсЙЉ4ЁС462kJЕФШШСП
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЗДгІ3A(g)+B(g)ЈT2C(g)дкШ§жжВЛЭЌЕФЬѕМўЯТНјааЗДгІЃЌдкЭЌвЛЪБМфФкЃЌВтЕУЕФЗДгІЫйТЪгУВЛЭЌЕФЮяжЪБэЪОЮЊЃКЂйvAЈT1mol/(Lmin)ЃЌЂкvCЈT0.5 mol/(Lmin)ЃЌЂлvBЈT0.5 mol/(Lmin)ЃЌШ§жжЧщПіЯТИУЗДгІЫйТЪДѓаЁЕФЙиЯЕе§ШЗЕФЪЧ(ЁЁЁЁ)
A. ЂкЃОЂлЃОЂйB. ЂйЃОЂкЃОЂлC. ЂлЃОЂйЃОЂкD. ЂкЃОЂйЃОЂл
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЕТЙњЛЏбЇМвЙўВЎ(F.Haber)Дг1902ФъПЊЪМбаОПгЩЕЊЦјКЭЧтЦјжБНгКЯГЩАБЁЃКЯГЩАБЮЊНтОіЪРНчЕФСИЪГЮЪЬтзїГіСЫживЊЙБЯзЁЃЦфдРэЮЊN2(g)+3H2(g)2NH3(g) ЁїH=-92.4kJ/mol
(1)ШєвбжЊH-HМќЕФМќФмЮЊ436.0kJ/molЃЌN-HЕФМќФмЮЊ390.8kJ/molЃЌдђN![]() NЕФМќФмдМЮЊ_____kJ/mol
NЕФМќФмдМЮЊ_____kJ/mol
(2)КЯГЩАБЗДгІВЛМгДпЛЏМСКмФбЗЂЩњЃЌДпЛЏМСЬњДЅУНМгШыКѓВЮгыСЫЗДгІНЕЕЭСЫЛюЛЏФмЁЃЦфФмСПдРэШчЭМЫљЪОЃЌдђМгСЫДпЛЏМСКѓећИіЗДгІЕФЫйТЪгЩ______ОіЖЈ(ЬюЁАЕквЛВНЗДгІЁБЛђепЁАЕкЖўВНЗДгІЁБ)ЃЌЮДЪЙгУДпЛЏМСЪБФцЗДгІЛюЛЏФм______е§ЗДгІЛюЛЏФм(ЬюЁАДѓгкЁБЁАаЁгкЁБЛђепЁАЕШгкЁБ)
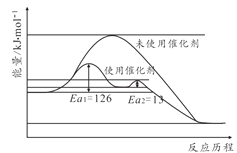
(3)ДгЦНКтКЭЫйТЪНЧЖШПМТЧЃЌЙЄвЕЩњВњВЩШЁ20MPaЕН50MPaЕФИпбЙКЯГЩАБдвђ______
(4)вЛЖЈЮТЖШЯТКуШнШнЦїжаЃЌвдВЛЭЌЕФH2КЭN2ЮяжЪЕФСПжЎБШМгШыЃЌЦНКтЪБNH3ЬхЛ§ЗжЪ§ШчЭМЫљЪОЃЌдђH2зЊЛЏТЪaЕу______bЕу(Ью"ДѓгкЁБЁАаЁгкЁБЛђепЁАЕШгкЁБ)ЁЃШєЦ№ЪМбЙЧПЮЊ20MPaЃЌдђbЕуЪБЬхЯЕЕФзмбЙЧПдМЮЊ______MPaЁЃ
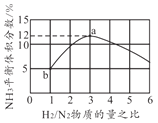
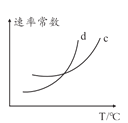
(5)ШєИУЗДгІЕФе§ФцЗДгІЫйТЪЗжБ№БэЪОЮЊvе§=Kе§![]() ЃЌvФц=KФцc2(NH3)ЃЌдђвЛЖЈЮТЖШЯТЃЌИУЗДгІ ЕФЦНКтГЃЪ§K=______(гУКЌKе§КЭKФцЕФБэДяЪНБэЪО)ЃЌШєKе§КЭKФцЖМЪЧЮТЖШЕФКЏЪ§ЃЌЧвЫцЮТЖШЩ§ИпЖјЩ§ИпЃЌдђЭМжаcКЭdЗжБ№БэЪО______КЭ______ЫцЮТЖШБфЛЏЧїЪЦ(ЬюKе§ЛђепKФц)ЁЃ
ЃЌvФц=KФцc2(NH3)ЃЌдђвЛЖЈЮТЖШЯТЃЌИУЗДгІ ЕФЦНКтГЃЪ§K=______(гУКЌKе§КЭKФцЕФБэДяЪНБэЪО)ЃЌШєKе§КЭKФцЖМЪЧЮТЖШЕФКЏЪ§ЃЌЧвЫцЮТЖШЩ§ИпЖјЩ§ИпЃЌдђЭМжаcКЭdЗжБ№БэЪО______КЭ______ЫцЮТЖШБфЛЏЧїЪЦ(ЬюKе§ЛђепKФц)ЁЃ
(6)ГЃЮТЯТЃЌЯђ20mLЕФ0.1mol/LЕФбЮЫсжаЭЈШывЛЖЈСПАБЦјЗДгІКѓШмвКГЪжаад(МйЩшШмвКЬхЛ§БфЛЏКіТдВЛМЦ)дђЫљЕУШмвКжаc(NH4+)=_______
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЮяжЪвЛЖЈЪєгкЭЌЯЕЮяЕФЪЧЃЈ ЃЉ
Ђй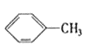 Ђк
Ђк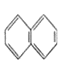 Ђл
Ђл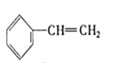 ЂмC2H4 ЂнCH2=CH-CH=CH2ЂоC3H6Ђп
ЂмC2H4 ЂнCH2=CH-CH=CH2ЂоC3H6Ђп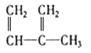 Ђр
Ђр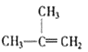
A. ЂмКЭЂрB. ЂйКЭЂлC. ЂнЁЂЂпКЭЂрD. ЂмЁЂЂоКЭЂр
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПОбаОПЗЂЯжАзвЯаХЯЂЫигаЃК![]() (2ЃЌ4-ЖўМзЛљ-1-И§ЯЉ)ЃЌ
(2ЃЌ4-ЖўМзЛљ-1-И§ЯЉ)ЃЌ![]() (3ЃЌ7-ЖўМзЛљ-1-аСЯЉ)ЃЌМвВЯЕФадаХЯЂЫиЮЊЃКCH3(CH2)8CH==CHЁЊCH==CH(CH2)8CH3ЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
(3ЃЌ7-ЖўМзЛљ-1-аСЯЉ)ЃЌМвВЯЕФадаХЯЂЫиЮЊЃКCH3(CH2)8CH==CHЁЊCH==CH(CH2)8CH3ЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
AЃЎ2ЃЌ4-ЖўМзЛљ1И§ЯЉЕФЗжзгЪНЮЊC9H18
BЃЎ2ЃЌ4-ЖўМзЛљ-1-И§ЯЉгы3ЃЌ7-ЖўМзЛљ-1-аСЯЉЛЅЮЊЭЌЯЕЮя
CЃЎвдЩЯШ§жжаХЯЂЫиОљФмЪЙфхЕФЫФТШЛЏЬМШмвКЭЪЩЋ
DЃЎ1 molМвВЯЕФадаХЯЂЫигы1 mol Br2МгГЩЃЌВњЮяжЛгавЛжж
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЂё.ФГЬўЕФНсЙЙМђЪНЮЊ
![]()
ЃЈ1ЃЉИУЬўЕФУћГЦЮЊ_______________ЁЃ
ЃЈ2ЃЉШєИУЬўЪЧгЩЯЉЬўЃЈКЌвЛИіЬМЬМЫЋМќЃЉКЭЧтЦјМгГЩЖјРДЃЌдђЯЉЬўЕФНсЙЙга_____жжЃЛШєИУЬўЪЧгЩФГШВЬўЃЈКЌвЛИіЬМЬМШ§МќЃЉКЭзуСПЧтЦјМгГЩЖјРДЃЌдђШВЬўЕФНсЙЙМђЪНЮЊ_______________ЁЃ
IIЃЎБъзМзДПіЯТЃЌ1.68 LЮоЩЋЮоЮЖЕФПЩШМадЦјЬхдкзуСПбѕЦјжаЭъШЋШМЩеЃЌШєНЋВњЮяЭЈШызуСПГЮЧхЪЏЛвЫЎЃЌЕУЕНЕФАзЩЋГСЕэжЪСПЮЊ15.0 gЃЛШєгУзуСПМюЪЏЛвЮќЪеШМЩеВњЮяЃЌдіжи9.3 gЁЃ
ЃЈ1ЃЉМЦЫуШМЩеВњЮяжаЫЎЕФжЪСПЮЊ_________ЁЃ
ЃЈ2ЃЉШєдЦјЬхЪЧЕЅвЛЕФЬўРрЦјЬхЃЌЭЈЙ§МЦЫуЭЦЖЯЫќЕФЗжзгЪНЃК_____________ЁЃ
ЃЈ3ЃЉШєдЦјЬхЪЧСНжжЕШЮяжЪЕФСПЕФЦјЬЌЬўЕФЛьКЯЮяЃЌЧыаДГіЫќУЧЕФНсЙЙМђЪН(вЊЧѓаДГівЛзщЗћКЯЬѕМўЕФЮяжЪЕФНсЙЙМђЪНМДПЩ)ЃК__________________ЁЁЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПАДвЊЧѓЬюПе
(1)1mol Na2O2ЙЬЬхгыЫЎЭъШЋЗДгІЪБзЊвЦЕФЕчзгЪ§_____________ЃЌЗДгІЕФРызгЗНГЬЪНЮЊ________________ЁЃ
(2)ЙЄвЕЩЯгЩЛдЭПѓЩњВњЭЕФжївЊЗДгІЮЊЃКCu2S+O2![]() 2Cu+SO2ЃЌИУЗДгІжаБЛЛЙдЕФдЊЫиЪЧ__________(ЬюдЊЫиЗћКХ)ЁЃ
2Cu+SO2ЃЌИУЗДгІжаБЛЛЙдЕФдЊЫиЪЧ__________(ЬюдЊЫиЗћКХ)ЁЃ
(3)ЗДгІ(2)жаВњЩњЕФSO2ЮВЦјПЩгУNaOHШмвКЮќЪеЃЌШєгУ1L 1mol/LЕФNaOHШмвКЮќЪеБъзМзДПіЯТ22.4L SO2ЃЌЗДгІЕФРызгЗНГЬЪНЮЊ____________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЭЌЮТЭЌбЙЯТЃЌЯТСаИїзщШШЛЏбЇЗНГЬЪНжаЃЌЁїH1ЃМЁїH2ЪЧЃЈ ЃЉ
A. C(s)ЃЋ![]() O2(g)ЃНCO(g)ЃЛЁїH1C(s)ЃЋO2(g)ЃНCO2(g)ЃЛЁїH2
O2(g)ЃНCO(g)ЃЛЁїH1C(s)ЃЋO2(g)ЃНCO2(g)ЃЛЁїH2
B. ![]() H2(g)ЃЋ
H2(g)ЃЋ![]() Cl2(g)ЃНHCl(g)ЃЛЁїH1 H2(g)ЃЋCl2(g)ЃН2HCl(g)ЃЛЁїH2
Cl2(g)ЃНHCl(g)ЃЛЁїH1 H2(g)ЃЋCl2(g)ЃН2HCl(g)ЃЛЁїH2
C. 2H2(g)ЃЋO2(g)ЃН2H2O(g)ЃЛЁїH1 2H2(g)ЃЋO2(g)ЃН2H2O(l)ЃЛЁїH2
D. S(g)ЃЋO2(g)ЃНSO2(g)ЃЛЁїH1 S(s)ЃЋO2(g)ЃНSO2(g)ЃЛ ЁїH2
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com