
Ϊ���ƴ����������������ڡ�ʮ���塱�ڼ䣬������CO2��Ϊȼ�ϻ��л���ѧ��Ʒ�Ĺ����Ϊ��ʵ������������(SO2)�ŷ�������8%����������(NOx)�ŷ�������10%��
I��Ŀǰ������������Ⱦ�ж��ַ�����
��1������NOx��һ�ַ��������ü������ԭNOx��д������ֱ�ӽ�NO2��ԭ�õ�����Ⱦ�IJ���Ļ�ѧ����ʽ ��
��2����������β���ķ���֮һ�����������ϰ�װ��
ת�������������·�Ӧ��
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)����H��0��
N2(g)+2CO2(g)����H��0��
�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK= ��
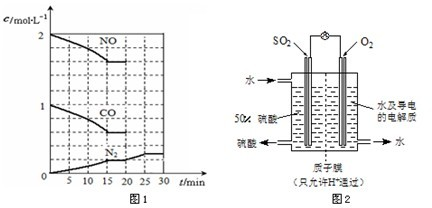
��һ���¶��£���2molNO��1molCO����1L
 �̶��ݻ��������У���Ӧ�����и����ʵ�Ũ�ȱ仯
�̶��ݻ��������У���Ӧ�����и����ʵ�Ũ�ȱ仯
����ͼ��ʾ��
�������¶Ȳ��䣬20minʱ���������г���
CO��N2��0.6mol��ƽ�⽫ �ƶ�������� �����ҡ���������
��20minʱ�ı䷴Ӧ����������N2Ũ�ȷ�������ͼ��ʾ�ı仯����ı����������
�� ������ţ���
�ټ�������� �ڽ����¶ȡ� ����С��������� ������CO2����
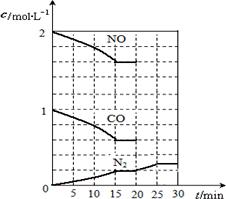
 ��3�������ij���е�λ���Ƴɹ�һ�ִ���SO2�ķ��������õ绯ѧԭ�������糧�����Ĵ���SO2�Ƴ����ᣬװ������ͼ�����ط�Ӧ����ʽΪ��2SO2��O2��2H2O��2H2SO4���õ�ص綯��Ϊ1.06V��ʵ�ʹ����У�д��������ӦʽΪ �������ַ�������SO2�������ŵ��ǿɻ��մ�����Ч�ܣ�����ƷΪH2SO4�����ٻ�����Ⱦ��
��3�������ij���е�λ���Ƴɹ�һ�ִ���SO2�ķ��������õ绯ѧԭ�������糧�����Ĵ���SO2�Ƴ����ᣬװ������ͼ�����ط�Ӧ����ʽΪ��2SO2��O2��2H2O��2H2SO4���õ�ص綯��Ϊ1.06V��ʵ�ʹ����У�д��������ӦʽΪ �������ַ�������SO2�������ŵ��ǿɻ��մ�����Ч�ܣ�����ƷΪH2SO4�����ٻ�����Ⱦ��
II�����������̼������Һ���շ��糧�����еĶ�������
��֪��H2SO3�ĵ���ƽ�ⳣ��Ϊ K1=1.54��10-2 ��K2=1.O2��10-7
H2CO3�ĵ���ƽ�ⳣ��ΪK1=4.31��l0-7 K2=5.61��10-11
��4����д����̼������Һ��ͨ��һ������SO2��������Ⱦ�Ķ�����̼����ĵĻ�ѧ����ʽ

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||

| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| 1 |
| 2 |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�������ʮ�������ص�ѧУ2012�������ҵ������(��)��ѧ���� ���ͣ�058
Ϊ���ƴ����������������ڡ�ʮ���塱�ڼ䣬������CO2��Ϊȼ�ϻ��л���ѧ��Ʒ�Ĺ����Ϊ��ʵ������������(SO2)�ŷ�������8������������(NOx)�ŷ�������10����
��һ�ֽ�CO2��Ϊȼ�ϻ��л���ѧ��Ʒ�Ĺ���ֳ�3�����裺
������Ũ̼�����Һ���տ����е�CO2��
�ڽ��ڢٲ�����Һ������H2��O2��ͬʱ�����CO2��
�۽��ڢڲ�������H2(g)��CO2(g)��һ��������ת����CH4(g)��H2O(l)��
��֪��H2(g)��![]() O2(g)��H2O(l)����H1����285.8 kJ/mol
O2(g)��H2O(l)����H1����285.8 kJ/mol
CH4(g)��2O2(g)��CO2(g)��2H2O(l)����H2����889.6 kJ/mol
д���ڢ۲���Ӧ���Ȼ�ѧ����ʽΪ________��
��Ŀǰ������������Ⱦ�ж��ַ�����
(1)����NOx��һ�ַ��������ü������ԭNOx��д������ֱ�ӽ�NO2��ԭ�õ�����Ⱦ�IJ���Ļ�ѧ����ʽ________��
(2)��������β���ķ���֮һ�����������ϰ�װ��ת�������������·�Ӧ��
2NO(g)��2CO(g)�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��________��
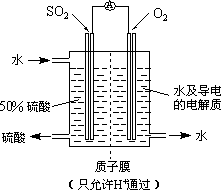
��һ���¶��£���2 mol��NO��1 mol��CO����1 L�̶��ݻ��������У���Ӧ�����и����ʵ�Ũ�ȱ仯����ͼ��ʾ��
�������¶Ȳ��䣬20 minʱ���������г���CO��N2��0.6 mol��ƽ�⽫________�ƶ�(����������ҡ�����)��
��20 minʱ�ı䷴Ӧ����������N2Ũ�ȷ�������ͼ��ʾ�ı仯����ı������������________(�����)��
�ټ������
�ڽ����¶�
�����������
������CO2����
(3)�����ij���е�λ���Ƴɹ�һ�ִ���SO2�ķ��������õ绯ѧԭ�������糧�����Ĵ���SO2�Ƴ����ᣬװ����ͼ�����ط�Ӧ����ʽΪ��2SO2��O2��2H2O��2H2SO4���õ�ص綯��Ϊ1.06 V��ʵ�ʹ����У���SO2ͨ���ص�________��(���������)��������ӦʽΪ________�������ַ�������SO2�������ŵ��ǿɻ��մ�����Ч�ܣ�����ƷΪH2SO4�����ٻ�����Ⱦ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�꽭��ʡ�γ���ѧ�߶����ϣ����л�ѧ�Ծ������ޣ��������棩 ���ͣ������
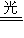 NO+O����2NO+O2=2NO2����O2+O=O3�����ܷ�Ӧ�ɱ�ʾΪ ��NO2���������� ���ã�
NO+O����2NO+O2=2NO2����O2+O=O3�����ܷ�Ӧ�ɱ�ʾΪ ��NO2���������� ���ã��鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com