
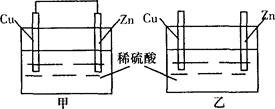
| A.甲装置中铜片表面有气泡生成 | B.乙装置中电能转化为化学能 |
| C.甲装置中电能转化为化学能 | D.乙装置中铜片表面有气泡生成 |
科目:高中化学 来源:不详 题型:单选题
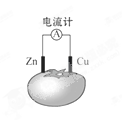
| A.一段时间后,锌片质量会变小 | B.铜电极附近会出现蓝色 |
| C.电子由铜通过导线流向锌 | D.锌电极是该电池的正极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
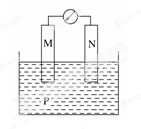
| | M | N | P |
| A | 锌 | 铜 | 稀硫酸溶液 |
| B | 铜 | 铁 | 稀盐酸溶液 |
| C | 银 | 锌 | 硝酸银溶液 |
| D | 锌 | 铁 | 硝酸铁溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶液的pH增大 |
| B.溶液中的Zn2+浓度增大 |
| C.溶液中的SO42— 浓度增大 |
| D.溶液的密度增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
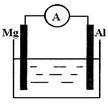
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原电池是把电能转化为化学能的装置 |
| B.原电池中电子流出的一极是正极 |
| C.原电池的两极发生的反应均为氧化还原反应 |
| D.形成原电池后,原电池中的阳离子移向正极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.①② | B.①②③ | C.②③④ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.正极附近的SO4 2- 离子浓度逐渐增大 | B.铜片上有H2逸出 |
| C.溶液的pH逐渐变小 | D.电子通过导线由铜片流向锌片 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com