
��ס��������º��ݵ��ܱ������У��ֱ����һ������A��B��������Ӧ��A(g)��B(g)  xC(g) ��H��0�������������c(A)��ʱ��t�ı仯��ͼ��ʾ��
xC(g) ��H��0�������������c(A)��ʱ��t�ı仯��ͼ��ʾ��
| ���� | �� | �� |
| �ݻ���L�� | 0.5 | 0.5 |
| ��Ӧ���ȣ�kJ�� | Q1 | Q2 |
| ��Ӧ����ʼ�� | 1 molA 1 molB | 0.5 molA 0.5 molB |
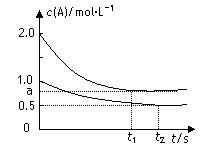

����˵����ȷ����
A��x=1 B��Q1��2Q2 C������������Ϣ������aֵ
D�����������������䣬��ʼʱ������������0.2 mol A��0.2 mol B��0.2 mol C�����ʱv(��)> v(��)
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�Ӹ����������ƶ�ϩ �������й������Ʋ⣬����ȷ���� ( )
�������й������Ʋ⣬����ȷ���� ( )
A��������ʹ���Ը��������Һ��ɫ
B��������ΪҺ̬��������ˮ
C������ʽΪC10H16
D������������CCl4��Һ��Ӧ���������ͼ

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
X��Y��Z��W��Ϊ������Ԫ�أ����������ڱ������λ����ͼ��ʾ����Yԭ�ӵ������������ڲ��������3��������˵����ȷ����
A��X����̬�⻯���Y���ȶ�
B��W������������Ӧˮ��������Ա�Z��ǿ
C��Z�ķǽ����Ա�Y��ǿ
D��X��Y�γɵĻ����ﶼ������ˮ

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��4molA�����2molB������2L���ܱ������л�ϣ���һ�������·������·�Ӧ��
2A(g)+B(g)  2C(g)������2�����C��Ũ��Ϊ0.6mol/L��
2C(g)������2�����C��Ũ��Ϊ0.6mol/L��
��1��2s����B��ʾ�ķ�Ӧ����
��2��2sʱA�����ʵ���Ũ��Ϊ
��3��2sʱB�����ʵ���Ϊ
��4������C��Ũ�� ����ܡ����ܡ����ﵽ2mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ����
A��������KMnO4��Һ��ͨ��SO2��3SO2+2MnO +4OH��=2MnO2��+3SO
+4OH��=2MnO2��+3SO +2H2O
+2H2O
B��������Һ��ˮ���е�CaCO3��Ӧ��CaCO3+2H+=Ca2++CO2��+H2O
C����FeBr2��Һ��ͨ������Cl2��2Fe2++Cl2=2Fe3++2Cl��
D��������Cu(OH)2�м�����ȩ��Һ�����ȣ�
CH3CHO+2Cu(OH)2+OH�� CH3COO��+Cu2O��+3H2O
CH3COO��+Cu2O��+3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ѣ�DME������Ϊ��21���͵����ȼ�ϡ����ɺϳ����Ʊ������ѵ���Ҫԭ�����£�
�� CO(g)+2H2(g) CH3OH(g) ��H 1=��90.7 kJ��mol-1
CH3OH(g) ��H 1=��90.7 kJ��mol-1
�� 2CH3OH(g) CH3OCH3(g)+H2O(g) ��H 2=��23.5 kJ��mol-1
CH3OCH3(g)+H2O(g) ��H 2=��23.5 kJ��mol-1
�� CO(g)+H2O(g) CO2(g)+H2(g) ��H 3=��41.2kJ��mol-1
CO2(g)+H2(g) ��H 3=��41.2kJ��mol-1
�ش��������⣺
��1����Ӧ3H2(g)��3CO(g) CH3OCH3(g)��CO2(g)�ġ�H�� �� kJ��mol-1��
CH3OCH3(g)��CO2(g)�ġ�H�� �� kJ��mol-1��
��2�����д�ʩ�У������CH3OCH3���ʵ��� �� ��
A��ʹ�ù�����CO B�������¶� C������ѹǿ
��3����Ӧ�������CH3OCH3�IJ��ʣ�ԭ���� �� ��
��4�����ϳ�����n(H2)/n(CO)=2ͨ��1 L�ķ�Ӧ���У�һ�������·�����Ӧ��
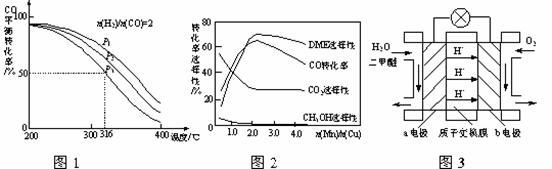
4H2(g)+2CO(g)  CH3OCH3(g)+H2O(g) ��H����CO��ƽ��ת�������¶ȡ�ѹǿ�仯��ϵ��ͼ1��ʾ������˵����ȷ���� �� ��
CH3OCH3(g)+H2O(g) ��H����CO��ƽ��ת�������¶ȡ�ѹǿ�仯��ϵ��ͼ1��ʾ������˵����ȷ���� �� ��
A����H <0
B��P1<P2<P3
C������P3��316��ʱ����ʼʱn(H2)/n(CO)=3����ﵽƽ��ʱ��COת����С��50��[
��5������һ�����͵Ĵ�������Ҫ�ɷ���Cu-Mn�ĺϽ𣩣�����CO��H2�Ʊ������ѡ��۲�ͼ2�ش����⡣������n(Mn)/n(Cu)ԼΪ �� ʱ�������ڶ����ѵĺϳɡ�
��6��ͼ3Ϊ��ɫ��Դ��������ȼ�ϵ�ء��Ĺ���ԭ��ʾ��ͼ��a�缫�ĵ缫��ӦʽΪ �� ��
��7���״�Һ����ˮ���ƶ����ѵ�ԭ���ǣ�CH3OH +H2SO4��CH3HSO4+H2O��
CH3 HSO4+CH3OH��CH3OCH3+H2SO4����ϳ����Ʊ������ѱȽϣ��ù��յ��ŵ��Ƿ�Ӧ�¶ȵͣ�ת���ʸߣ���ȱ���� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и��������У�����֮��ͨ��һ����Ӧ����ʵ��ͼʾ�仯����
| ���ʱ�� | ����ת����ϵ | a | b | c | d |
| �� |
| NO[] | NO2 | N2 | HNO3 |
| �� | Na2O | Na2O2 | Na | NaOH | |
| �� | FeCl2 | FeC13 | Fe | CuCl2 | |
| �� | Al2O3 | NaAlO2 | Al | Al(OH)3 |
A���٢ڢ� B���٢ۢ� C���ۢ� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й�ʵ��ԭ����ʵ�������������ȷ���� (����)��
 [
[
A������һ��������ͬ����ֽ����ƽ���������ϣ���NaOH�������������
����
B������ȥNO��������NO2�����������ͨ������NaOH��Һ
C��ʵ������ͼ1��ʾװ����ȡ��������
D��ʵ������ͼ2��ʾװ�ü�����ͷȼ�� ������SO2
������SO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ�������������ȷ����
A��������������ȼ�գ�������ɫ���棬ƿ���Ϸ��а�ɫ����
B����̼���ơ�̼�����Ƶı�����Һ�еμӷ�̪����ǰ����Һ���
C��ͭ��������ȼ�գ������ػ�ɫ��
D��������������Һ�еμ�ϡK3[Fe(CN)6]��Ϊ��������ɫ��Һ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com