
【题目】下列说法中正确的是( )
A. 生成物全部化学键形成所释放的能量大于破坏反应物全部化学键所吸收的能量时, 反应为吸热反应
B. 向Na2CO3溶液中加少量BaCl2固体,CO32-的水解程度变小
C. 在FeCl3+3KSCN![]() 3KCl+Fe(SCN)3体系中加入KI固体,平衡不移动
3KCl+Fe(SCN)3体系中加入KI固体,平衡不移动
D. 对一个可逆反应来说,吸热反应一方的速率受温度变化的影响总是大于放热反应
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】汽车尾气中含有上百种不同的化合物,其中的污染物有固体悬浮颗粒、一氧化碳、二氧化碳、碳氢化合物、氮氧化合物、铅及硫氧化合物等,一辆轿车一年排放的有害废气比自身重量大3倍。其中NO气体是由于内燃机燃烧的高温引起N2和O2反应所致:N2(g)+O2(g)![]() 2NO(g) △H>0,已知该反应在2404℃时,平衡常数K=64×10-4。请回答:
2NO(g) △H>0,已知该反应在2404℃时,平衡常数K=64×10-4。请回答:
(1)某温度下,向4L密闭容器中充入N2和O2各4mol,平衡时,5分钟后O2的物质的量为1mol,则N2的反应速率是____________。
(2)恒容条件下,判断该反应达到平衡的标志是________。(填字母序号)。
A.消耗1mol N2同时生成1mol O2 B.混合气体密度不变
C.混合气体平均相对分子质量不变 D.2v(N2)正=v(NO)逆
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是________(填字母序号)。

(4)可逆反应N2(g)+O2(g)![]() 2NO(g)的平衡常数表达式为____________。温度升高,平衡常数将会
2NO(g)的平衡常数表达式为____________。温度升高,平衡常数将会
_____________(填“增大、或“减小”)
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol·L-1、4.0×10-2mol·L-1和3.0×10-3mol·L-1,此时反应___________(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”)。
(6) 火箭燃料N2H4(肼)在NO2中燃烧,生成N2、液态水。已知:
N2(g)+2O2(g)=2NO2(g) △H1=+67kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(l) △H2=-534kJ/mol
由此请写出发射火箭时燃烧反应的热化学方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中,用铜铬的氧化物作催化剂,用一定量的HCl(g)和O2制取Cl2的原理为:4HCl(g)+O2(g) ![]() 2Cl2(g)+2H2O(g) ΔH<0。下列有关说法不正确的是
2Cl2(g)+2H2O(g) ΔH<0。下列有关说法不正确的是
A. 平衡前,随着反应的进行,容器内压强变小
B. 平衡时,其他条件不变,分离出H2O(g),逆反应速率减小
C. 平衡时,其他条件不变,升高温度平衡常数增大
D. 其他条件不变,使用不同催化剂,HCl(g)的转化率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,C、D、E、F、X、Y都是惰性电极。将电源接通后,向(乙)中滴入酚酞溶液,在 F极附近显红色.则下列说法正确的是

A.若用乙烷、空气燃料电池作电源,电解质为KOH溶液,则B极的电极反应式为:O2+2H2O+4e-=4OH-
B.欲用(丙)装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液
C.(丁)装置中Y极附近红褐色变深,说明氢氧化铁胶粒带正电荷
D.C、D、E、F电极均有单质生成,其物质的量比为1∶1∶2∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各图均能表示甲烷的分子结构,按要求回答下列问题。
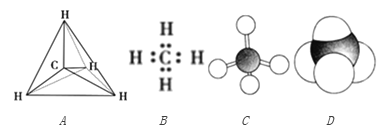
(1)甲烷的比例模型是________,甲烷的电子式是__________ (填序号)。
(2)写出甲烷与氯气发生反应的化学方程式_____________(只写第一步),该反应的反应类型是________________。
(3)相对分子质量为100的烷烃的分子式是_______________。
(4)甲烷与丙烷互为________。
A. 同位素 B. 同素异形体 C. 同系物 D. 同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组在实验室制取乙酸乙酯的主要步骤如下:
①配制2mL浓硫酸、3mL乙醇(含18O)和2mL乙酸的混合溶液
②按如图连接好装置并加入混合液,用小火均匀加热3~5min
③待试管乙收集到一定量产物后停止加热,撤出试管乙用力振荡,然后静置待分层
 ④分离出乙酸乙酯,洗涤、干燥。
④分离出乙酸乙酯,洗涤、干燥。
回答问题:
(1)装置中球形干燥管,除起冷凝作用外,另一重要作用是____________________。
(2)步骤(2)安装好实验装置,加入样品前还应检查____________________。
(3)反应中浓硫酸的作用是______________________;
写出能表示18O位置的制取乙酸乙酯的化学方程式________________________。
(4)上述实验中饱和碳酸钠溶液的作用是(填字母)_____________。
A.中和乙酸并吸收乙醇 B.中和乙酸和乙醇
C.加速酯的生成,提高其产率 D.减少乙酸乙酯的溶解
(5)从试管乙中分离出乙酸乙酯的实验操作名称是 __________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油裂解可获得 A。已知 A 在通常状况下是一种相对分子量为 28 的气体,A 通过加聚反应可以得到 F,F 常作为食品包装袋的材料。有机物 A、B、C、D、E、F 有如下图的关系。
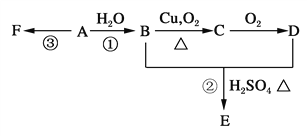
(1)C的结构简式为___________________。
(2)写出反应①的化学方程式___________________。
(3)写出反应②的化学方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性。回答下列问题:
(1)①H3PO2属于一元中强酸,酸性略强于亚硫酸,写出其电离方程式_________
②下列说法正确的是_________
A.NaH2PO2溶液显弱碱性
B.向NaH2PO2溶液中滴加硝酸可以制得H3PO2
C.1molH3PO2最多可以和3molNaOH发生反应
D.NaH2PO2溶液中:c(Na+)=c(H3PO2)+c(H2PO2-)
(2)H3PO2可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳离子交换膜和阴离子交换膜分别只允许阳离子、阴离子通过):

①写出阳极反应式_________
②A、B、C分别是_________离子交换膜、_________离子交换膜、_________离子交换膜(填“阴”或“阳”)
③阳极室中溶液pH _________(填变大、变小或不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释,pH随溶液体积的变化曲线如下图所示。下列说法正确的是( )

A. HA的酸性比HB的酸性弱
B. a点溶液的导电性比c点溶液的导电性弱
C. 若两溶液无限稀释,则它们的c(H+)相等
D. 对a、b两点溶液同时升高温度,则c(A-)/ c(B-)增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com