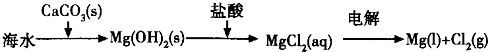
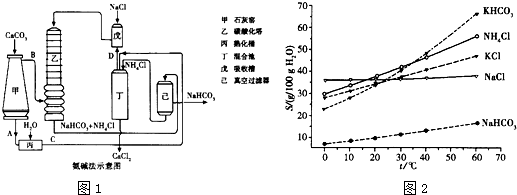
铝和浓H2SO4反应的实验设计如下:
①把铝条表面的氧化膜用砂纸擦掉洗净后,将其插入盛浓H2SO4的试管中,期间没有观察到明显现象,1 min~2 min后取出。
②把①中的铝条用水冲洗后迅速放入饱和CuSO4溶液中,过一会儿取出,也没有观察到明显现象。
③把铝条表面的氧化膜用砂纸擦掉洗净后,迅速置于盛饱和CuSO4溶液的试管中,过一会儿取出,铝条表面覆盖有红色金属铜:2Al+3Cu2+=2Al3++3Cu。
④把①中铝条置于浓H2SO4中,加热,观察到铝条逐渐溶解并有刺激性气味的气体放出,此气体通入品红溶液中品红褪色。
根据上述现象回答下列问题:
(1)铝条能和CuSO4溶液反应生成铜的原因是______________________________。
(2)从实验现象判断常温下铝和浓硫酸_______(填“发生”或“不发生”)反应,理由是_______________
_____________________________________________。
(3)加热时铝和足量浓硫酸反应的化学方程式为_____________________________________________。
(1)铝的还原性比铜强
(2)发生;铝条浸入浓硫酸中没有明显现象,但取出铝条再浸入硫酸铜溶液,其表面无红色物质析出。②、③对比,在①中一定发生了某种反应,这种反应是由于浓H
2SO
4有强氧化性,将Al表面氧化生成一层致密的氧化物薄膜,阻止内部金属继续跟浓H
2SO
4反应,这种现象称为“钝化”
(3)2Al+6H
2SO
4(浓)
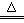
Al
2(SO
4)
3+3SO
2↑+6H
2O