
| A.将浓硝酸保存在棕色玻璃瓶中 |
| B.用镊子取出白磷并置于水中切割 |
| C.把氯酸钾制氧气后的残渣倒入垃圾桶 |
| D.氢气还原氧化铜实验先加热再通氢气 |
 CaCl2+2NH3↑+2H2O(2分)
CaCl2+2NH3↑+2H2O(2分) CaCl2+2NH3↑+2H2O(2)NH3易溶于水,NO2与水反应,不能用排水法收集,CO2、H2也可用排气法收集,所以只有NO只能用排水法收集,因为NO与空气中的氧气反应生成二氧化氮,不能用排气法收集,答案选b。
CaCl2+2NH3↑+2H2O(2)NH3易溶于水,NO2与水反应,不能用排水法收集,CO2、H2也可用排气法收集,所以只有NO只能用排水法收集,因为NO与空气中的氧气反应生成二氧化氮,不能用排气法收集,答案选b。

科目:高中化学 来源:不详 题型:单选题
| A.0.5a mol | B.2a mol | C.0.1a mol | D.(0.1+a)mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
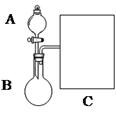
| 实验步骤 | 实验操作 | 预期现象及结论(步骤1只填现象) |
| 1 | 在A、B两支洁净的试管中各入1mL 2%的AgNO3溶液,然后边振荡试管边逐滴滴入2%稀氨水,至最初产生的沉淀恰好完全溶解,此时制得pH均约为8的银氨溶液。 | |
| 2 | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.对工业生产硝酸产生的废气、废水进行严格处理 |
| B.利用根瘤菌固氮以减少氮肥生产厂 |
| C.实验室制备NO2时在通风橱内进行 |
| D.建设“花园式工厂” |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
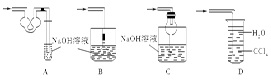
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
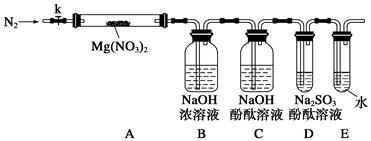
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 mol NH5中含有5NA个N—H键(NA表示阿伏加德罗常数) |
| B.NH5中既有共价键又有离子键,它形成的晶体是离子晶体 |
C.NH5的电子式为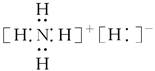 |
| D.它与水反应的化学方程式为:NH5+H2O=NH3·H2O+H2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入足量的新制氯水,溶液颜色变深,则含有Br- |
| B.加入KMnO4酸性溶液,溶液颜色褪去,则含有Br- |
| C.加入少量的碘水,再加入CCl4振荡,CCl4层有色,则含有Br- |
| D.加入足量FeCl3溶液,用CCl4萃取后,在无色的水层中加入氯水,溶液呈橙黄色,则含有Br- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com