
| A. | -386kJ•mol-1 | B. | +386kJ•mol-1 | C. | -746kJ•mol-1 | D. | +746kJ•mol-1 |
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:多选题
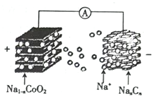 室温钠离子电池具有资源丰富,成本低,能量转换效率高、寿命等优势.一种用碳基材料(NaxCn)作负极的可充电钠离子电池的瓜原理如下:
室温钠离子电池具有资源丰富,成本低,能量转换效率高、寿命等优势.一种用碳基材料(NaxCn)作负极的可充电钠离子电池的瓜原理如下:| A. | 充电时,Na+向正极移动 | |
| B. | 放电时,负极的电极反应式为NaxCn-xe-=xNa++Cn | |
| C. | 充电时,阴极质量减小 | |
| D. | 充电时,阳极的电极反应式为NaCoO2-xe-=Na1-xCoO2+xNa+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
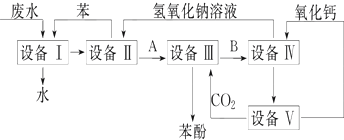
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和甲苯都能使酸性KMnO4溶液褪色 | |
| B. | 氯乙烯、聚乙烯、苯乙烯都是不饱和烃 | |
| C. | CH2=CH2和CH3CH2Cl都属于烃 | |
| D. | C2H4和C4H8一定都能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 水的电离平衡曲线如图所示:
水的电离平衡曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室少量金属钠保存在煤油中 | |
| B. | 从锂到铯,金属性逐渐减弱 | |
| C. | 金属钠与水反应时放出氢气 | |
| D. | 从锂到铯,单质与水反应越来越剧烈 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| T | M层上电子数是K层上电子数的3倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
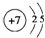 ,与氢元素形成一种离子YH4+,写出某溶液中含有该微粒的检验方法取少量样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子.
,与氢元素形成一种离子YH4+,写出某溶液中含有该微粒的检验方法取少量样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中NF3是氧化剂,H2O是还原剂 | |
| B. | NF3在潮湿空气中泄漏会产生无色气体 | |
| C. | 反应中还原剂与氧化剂的物质的量之比为1:2 | |
| D. | 若反应中生成0.1 mol HNO3,则反应共转移0.1 mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com