
| | X | Y | Z | M | R | Q |
| 原子半径/nm | | | 0.186 | 0.074 | 0.099 | 0.143 |
| 主要化合价 | | -4,+4 | | -2 | -1,+7 | +3 |
| 其它 | 阳离子核外无电子 | 可做半导体材料 | 焰色反应呈黄色 | | | |
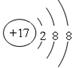 ;同位素(2)O2、 O3 (注:本整小题合计共2分,错一个不给分。) (3)2Na+2H2O=2NaOH+H2↑(2分)
;同位素(2)O2、 O3 (注:本整小题合计共2分,错一个不给分。) (3)2Na+2H2O=2NaOH+H2↑(2分)

科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.XY | B.XY2 | C.XY3 | D.XY4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2S、H2O、HF的稳定性依次增强 |
| B.Na+、Mg2+、Al3+的氧化性依次减弱 |
| C.H2SiO3、H2CO3、H2SO4的酸性依次增强 |
| D.KOH、NaOH、Mg(OH)2的碱性依次减弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Ge的电负性为1.8,则其是典型的非金属 |
| B.L层不含s能级,M层存在3f能级 |
| C.焰火是焰色反应,都是电子由基态跃迁到激发态的结果 |
| D.在电子云示意图中,小黑点是电子在原子核外出现的概率密度的形象描述 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③④ | B.①②④ | C.③④ | D.②⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.气态氢化物的稳定性:XH4>YH3>H2Z; |
| B.元素非金属性强弱关系:X>Y>Z |
| C.最高价氧化物对应水化物酸性:H2XO3>H3YO4>H2ZO4 |
| D.原子半径:X>Y>Z |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com