
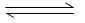
 2 NH3��g����H����92kJ�� mol-1�������Ϊ10L�ĺ����ܱ������г���1.2 mol N2��0.6molH 2��Ӧ����ͼ�����������������ȷ����
2 NH3��g����H����92kJ�� mol-1�������Ϊ10L�ĺ����ܱ������г���1.2 mol N2��0.6molH 2��Ӧ����ͼ�����������������ȷ����
| A��10��11min�÷�Ӧ������Ϊv(H2)>0.003mol/(L��min) |
| B�����ı����ô���ʱ����H �ᷢ���仯 |
| C�����������ܱ��������������ܱ������������������䣬NH3�IJ��ʽ����� |
| D����11min�������������䣬ѹ���������������c(H2 )�ı仯����Ϊb |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 bB��������ƽ������¶Ȳ��䣬�������������1�������ﵽ��ƽ��ʱ��B��Ũ����ԭ����60%������˵����ȷ���ǣ�
bB��������ƽ������¶Ȳ��䣬�������������1�������ﵽ��ƽ��ʱ��B��Ũ����ԭ����60%������˵����ȷ���ǣ�| A��ƽ�����淴Ӧ�����ƶ��ˣ� | B������A��ת���ʼ����ˣ� |
| C������B���������������ˣ� | D��a>b�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
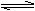 2 Z(g)+W(g)�� A���ֺ�ѹ��B���ֺ��ݣ���ƽ��ʱ��A�����Ϊ1.4a L ������˵���������
2 Z(g)+W(g)�� A���ֺ�ѹ��B���ֺ��ݣ���ƽ��ʱ��A�����Ϊ1.4a L ������˵���������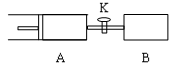
 ��v(A)
��v(A) �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
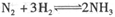 ����t1ʱ�̴ﵽƽ�⡣�����¶Ⱥ�ѹǿ���䣬��t2ʱ�̣���ͨ��һ����NH3����Ӧ����(v)��ʱ��(t)�Ĺ�ϵ������ȷ����(����)
����t1ʱ�̴ﵽƽ�⡣�����¶Ⱥ�ѹǿ���䣬��t2ʱ�̣���ͨ��һ����NH3����Ӧ����(v)��ʱ��(t)�Ĺ�ϵ������ȷ����(����)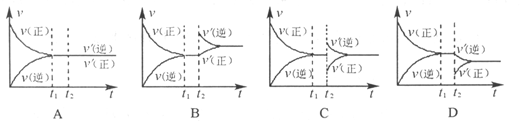
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���÷�Ӧ��ƽ�ⳣ������ʽK��c(H2O)/c(H2) |
| B����������������ܶȻ�ѹǿ���ֲ��䣬��˵���÷�Ӧ�Ѵﵽƽ��״̬ |
| C����Na2SO4�������ı���ʼ����H2��Ũ�ȣ���ƽ��ʱH2��ת���ʲ��� |
| D������ʼʱͶ��2.84gNa2SO4��һ����H2����Ӧ��ƽ��ʱ�����ڹ��干��2.264g����Na2SO4��ת����Ϊ45% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z(g) + W(s) ��H>0������������ȷ����
2Z(g) + W(s) ��H>0������������ȷ����| A����������W���淴Ӧ�������� | B��������������ѹǿ����ʱ����Ӧ�ﵽƽ�� |
| C��ʹ�ø�Ч������X��ת�������� | D�������¶ȣ�ƽ�������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CH3CH2OH��g����3H2O��g�������¶�ΪT��,�ݻ�������ܱ������У���3molH2��1molCO2��ϣ��ﵽƽ��ʱ�Ҵ�������������Ϊa,�����й�˵����ȷ����
CH3CH2OH��g����3H2O��g�������¶�ΪT��,�ݻ�������ܱ������У���3molH2��1molCO2��ϣ��ﵽƽ��ʱ�Ҵ�������������Ϊa,�����й�˵����ȷ����| A�������¶ȣ��÷�Ӧ��ƽ�ⳣ�������� |
| B������������г���1molH2��1molCO2���ﵽƽ��ʱ��H2��ת���ʽ�����CO2 |
| C������������ƽ�������з����ˮ�����������CO2��H2�������� |
| D��T��,���ݻ��ɱ���ܱ������н�3molH2��1molCO2��ϣ��ﵽƽ��ʱ�Ҵ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ﵽ��ѧƽ��ʱ����Ӧ������ȫת��Ϊ������ |
| B����ѧƽ����һ�������µ�ƽ�⣬�������ı�ʱ��ƽ����ܻ���ƻ� |
| C�����ﵽ��ѧƽ��ʱ����Ӧ������и��ɷֵ�Ũ����� |
| D�����ﵽ��ѧƽ��ʱ�����淴Ӧ����ֹͣ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

 4 C(g)���ﵽƽ��ʱ�������ʵ����ʵ���֮��Ϊn(A)��n(B)��n(C)=2��2��1����A����������Ϊw%�������¶Ȳ��䣬�ٳ���A��B��C�����ʵ����ֱ�Ϊa��b��c��������˵����ȷ����
4 C(g)���ﵽƽ��ʱ�������ʵ����ʵ���֮��Ϊn(A)��n(B)��n(C)=2��2��1����A����������Ϊw%�������¶Ȳ��䣬�ٳ���A��B��C�����ʵ����ֱ�Ϊa��b��c��������˵����ȷ���� ������С��w%
������С��w%�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com