
【题目】某汽车安全气囊的产气药剂主要含有 NaN3、Fe2O3、KClO4、NaHCO3 等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1) NaN3 是气体发生剂,受热分解产生 N2 和 Na,N2 的电子式为___________________。
(2) Fe2O3是主氧化剂,与 Na 反应生成的还原产物为_____________ (已知该反应为置换反应)。
(3) KClO4是助氧化剂,反应过程中与 Na 作用生成 KCl 和 Na2O。KClO4 含有化学键的类型为_____________________,K 的原子结构示意图为________________。
【答案】:NN: Fe 离子键和共价键 · ·
·
【解析】
(1)N2分子中N原子之间形成3对共用电子对,据此书写其电子式;
(2)Fe2O3是氧化剂,与Na发生置换反应,据此分析;
(3)KClO4由钾离子与高氯酸根离子构成,据此分析其所含的化学键;K原子质子数为19原子核外有4个电子层,据此分析。
(1)由8电子结构可知,N2分子中N原子之间形成3对共用电子对,其电子式为::NN:;故答案::NN:;
(2)Fe2O3是主氧化剂,与Na发生置换反应,Fe元素发生还原反应,则还原产物为Fe,故答案:Fe;
(3)KClO4由钾离子与高氯酸根离子构成,高氯酸根离子中Cl原子与O原子之间形成共价键,即该物质含有离子键、共价键;K原子质子数为19,原子核外有4个电子层,各层电子数为2、8、8、1;
故答案:离子键和共价键; 。
。


科目:高中化学 来源: 题型:
【题目】(一)碳酸镧![]() 可用于治疗终末期肾病患者的高磷酸盐血症,制备反应原理为:2LaCl3+6NH4HCO3═La2(CO3)3↓+6NH4Cl+3CO2↑+3H2O;某化学兴趣小组利用下列装置实验室中模拟制备碳酸镧。
可用于治疗终末期肾病患者的高磷酸盐血症,制备反应原理为:2LaCl3+6NH4HCO3═La2(CO3)3↓+6NH4Cl+3CO2↑+3H2O;某化学兴趣小组利用下列装置实验室中模拟制备碳酸镧。

(1)制备碳酸镧实验流程中导管从左向右的连接顺序为:F→_____→_____→_____→_____→_____;
(2)Y中发生反应的化学反应式为_______________;
(3)X中盛放的试剂是___________,其作用为___________________;
(4)Z中应先通入![]() ,后通入过量的
,后通入过量的![]() ,原因为__________________;
,原因为__________________;
二、氢氧化铈![]() 是一种重要的稀土氢氧化物,它可由氟碳酸铈精矿(主要含
是一种重要的稀土氢氧化物,它可由氟碳酸铈精矿(主要含![]() )经如下流程获得:
)经如下流程获得:

已知:在酸性溶液中![]() 有强氧化性,回答下列问题:
有强氧化性,回答下列问题:
(5)氧化焙烧生成的铈化合物二氧化铈(![]() ),其在酸浸时反应的离子方程式为_________________;
),其在酸浸时反应的离子方程式为_________________;
(6)已知有机物HT能将![]() 从水溶液中萃取出来,该过程可表示为:
从水溶液中萃取出来,该过程可表示为:![]() (水层)+
(水层)+![]() (有机层)
(有机层)![]()
![]() +
+![]() (水层)从平衡角度解释:向
(水层)从平衡角度解释:向![]() (有机层)加入
(有机层)加入![]() 获得较纯的含
获得较纯的含![]() 的水溶液的原因是________________;
的水溶液的原因是________________;
(7)已知298K时,Ksp[Ce(OH)3]=1×10-20,为了使溶液中![]() 沉淀完全,需调节pH至少为________;
沉淀完全,需调节pH至少为________;
(8)取某![]() 产品0.50g,加硫酸溶解后,用
产品0.50g,加硫酸溶解后,用![]() 的
的![]() 溶液滴定至终点(铈被还原成
溶液滴定至终点(铈被还原成![]() ).(已知:
).(已知:![]() 的相对分子质量为208)
的相对分子质量为208)
①![]() 溶液盛放在________(填“酸式”或“碱式”)滴定管中;
溶液盛放在________(填“酸式”或“碱式”)滴定管中;
②根据下表实验数据计算![]() 产品的纯度____________;
产品的纯度____________;
滴定次数 |
| |
滴定前读数 | 滴定后读数 | |
第一次 | 0.50 | 23.60 |
第二次 | 1.00 | 26.30 |
第三次 | 1.20 | 24.10 |
③若用硫酸酸化后改用![]() 的
的![]() 溶液滴定产品从而测定
溶液滴定产品从而测定![]() 产品的纯度,其它操作都正确,则测定的
产品的纯度,其它操作都正确,则测定的![]() 产品的纯度____________(填“偏高”、“偏低”或“无影响”)。
产品的纯度____________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴丙胺太林片是一种用于治疗胃肠痉挛性疼痛的药物,其合成路线如下:

回答下列问题:
(1)A→B的反应类型___________反应;F→G的反应类型________反应。
(2)C含有的官能团名称______________________________________。
(3)C→D的化学反应方程式___________________________________。
(4)E→F的化学反应方程式_____________________________________。
(5)I的结构简式是_____________________________________________。
(6)假设有机物J苯环上的氢化学环境相同,则J核磁共振氢谱有______组峰。
(7)写出1种与NaOH物质的量比1:3发生反应的E的同分异构体的结构简式____________。
(8)将下列合成路线补充完整

该路线中化合物X为______________;化合物Y为:___________________;试剂与条件a为:__________________、__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解足量下列溶液一段时间后,再加入一定量括号内的纯净物,能使溶液恢复到原来的成分和浓度的是
A. AgNO3[AgNO3] B. NaOH[NaOH] C. KCl[H2O] D. CuSO4[CuO]
【答案】D
【解析】石墨电极为惰性电极,溶液中阳离子在阴极放电,阴离子在阳极放电。A、电解AgNO3溶液,Ag+在阴极放电生成Ag,OH-在阳极放电生成O2,且n(Ag)∶n(O2)=2∶1,则应加入Ag2O恢复浓度,故A错误;B、电解NaOH溶液,H+在阴极放电生成H2,OH-在阳极放电生成O2,且n(H2)∶n(O2)=2∶1,则应加入一定量的H2O恢复原样,故B错误;C、电解KCl溶液,H+在阴极放电生成H2,Cl-在阳极放电生成Cl2,且n(H2)∶n(Cl2)=1∶1,则应加入一定量HCl恢复原样,故C错误;D、电解CuSO4溶液,Cu2+在阴极放电生成Cu,OH-在阳极放电生成O2,且n(Cu)∶n(O2)=2∶1,则应加入一定量CuO恢复原样,故D正确。故选D。
点睛:分析电解反应的原理,在两极析出什么物质(固体或气体),相当于什么物质脱离反应体系,根据元素守恒和原子比例,加入对应的物质,即可使溶液完全复原。
【题型】单选题
【结束】
28
【题目】工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的是

已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A. 碳棒上发生的电极反应:4OH--4e-=O2↑+2H2O
B. 电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C. 为了提高Ni的产率,电解过程中需要控制废水pH
D. 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,a、b、c、d、e 为元素周期表中前 4 周期的一部分元素,下列有关叙述正确的是( )

A.元素 b 位于第ⅥA 族,有+6、-2 价两种常见化合价
B.五种元素中,元素 e 的性质最稳定
C.元素 c 和 d 的最高价氧化物对应的水化物的酸性:c>d
D.元素 c 和 e 的气态氢化物的稳定性:c>e
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
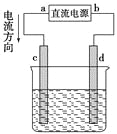
A. a为负极,b为正极
B. a为阳极,b为阴极
C. 电解过程中,d电极质量增加
D. 电解过程中,氯离子浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是某同学的化学笔记,需要改正的是
A.实验后剩余的钠粒,不能放回原试剂瓶中
B.在自然界中,钠元素和氯元素只以化合态存在
C.Na2O2可作为呼吸面具里氧气的来源
D.盐酸的工业制法:H2+Cl2![]() 2HCl
2HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(NH4)2Fe(SO4)26H2O(M=392g/mol)又称摩尔盐,简称FAS,它是浅蓝色绿色晶体,可溶于水,难溶于水乙醇。某小组利用工业废铁屑进行下列实验。请按要求回答下列问题:
Ⅰ. FAS的制取。流程如下:

(1)步骤①加热的目的是_________________________。
(2)步骤②必须在剩余少量铁屑时进行过滤,其原因是(用离子方程式表示): ______________。
Ⅱ.NH4+含量的测定。装置如图所示:

实验步骤:①称取FAS样品a g,加水溶解后,将溶液注入Y中
②量取b mL c1 mol/LH2SO4溶液于Z中
③向Y加入足量NaOH浓溶液,充分反应后通入气体N2,加热(假设氨完全蒸出),蒸氨结束后取下Z。
④用c2mol/LNaOH标准溶液滴定Z中过量的硫酸,滴定终点时消耗d mLNaOH标准溶液。
(3)仪器X的名称______________;N2的电子式为______________。
(4)步骤③蒸氨结束后,为了减少实验误差,还需要对直形冷凝管进行处理的操作是__________________;NH4+质量百分含量为(用代数式表示)__________________。
Ⅲ. FAS纯度的测定。称取FAS m g样品配制成500 mL待测溶液。分别取20.00mL待测溶液,进行如下方案实验:
(5)方案一:用0.01000mol/L的酸性KMnO4溶液进行滴定。滴定过程中需用到的仪器中(填图中序号)_________。滴定中反应的离子方程式为____________________。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
① ② ③ ④ ⑤ ⑥ ⑦ ⑧
(6)方案二: 待测液 ![]() 固体n g ;则FAS的质量百分含量为(用代数式表示)_____________________________。
固体n g ;则FAS的质量百分含量为(用代数式表示)_____________________________。
(7)方案一、二实验操作均正确,却发现方案一测定结果总是小于方案二的,其可能的原因是_______________;为验证该猜测正确,设计后续实验操作为_________________,现象为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学实验兴趣小组探究实验室中制备 Cl2 的过程,为证明过程中有水蒸气和 HCl 挥发出来,同时证明Cl2的某些性质,甲同学设计了如下图所示的实验装置,按要求回答问题。

(1)用浓盐酸与足量的 MnO2 反应制Cl2 的化学反应方程式_____。
(2)①装置 B 中盛放的试剂名称为_____,作用是_____,现象是_____。
②装置 D 和E 中出现的不同现象说明的问题是_________。
③装置 F 的作用是_____。
④写出装置G 中发生反应的离子方程式_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com