



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
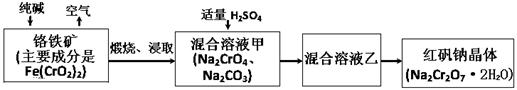
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na2O2�������������ǻ�ԭ�� |
| B��Fe2O3�ڷ�Ӧ�еõ����� |
| C��3 mol Na2O2������Ӧ����12 mol e������ת�� |
| D��Na2FeO4������ɱ�����������ǿ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢ڢܢ� | B���٢ۢ� |
| C���٢ڢۢ� | D��ֻ�Т٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na2O2�������������ǻ�ԭ�� |
| B��Na2FeO4���������������ǻ�ԭ���� |
| C��3 mol Na2O2������Ӧ����12 mol����ת�� |
| D����Na2FeO4��FeΪ��4�ۣ�����ǿ�����ԣ�������ɱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

 Cu2O��H2������ʯīӦ���Դ��________��������ͭ�缫�ϵĵ缫��ӦʽΪ________���������У���������Χ��ҺpH________(��������С�����䡱)��
Cu2O��H2������ʯīӦ���Դ��________��������ͭ�缫�ϵĵ缫��ӦʽΪ________���������У���������Χ��ҺpH________(��������С�����䡱)���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2CrO42-+2H+����д����ƽ���ƽ�ⳣ������ʽK= ����������ˮϡ�ͣ�ƽ�⽫ �ƶ�(���������������)��
2CrO42-+2H+����д����ƽ���ƽ�ⳣ������ʽK= ����������ˮϡ�ͣ�ƽ�⽫ �ƶ�(���������������)���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 (NxOy)�� H2O(��ƽʱx��y�þ�����ֵ��ʾ����������
(NxOy)�� H2O(��ƽʱx��y�þ�����ֵ��ʾ���������� ��)��
��)���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO(NH2)2 (l��+ H2O (l)��
CO(NH2)2 (l��+ H2O (l)��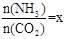 ����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��
����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��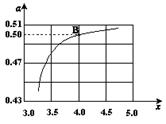
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������AΪ��������������Ļ���� |
| B������A�ж�������������������Ϊ4��1 |
| C����Ӧ�й�����п95��5g |
| D����Ӧ�й�ת�Ƶ���1��5mol |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com