
(15分)有机化学
已知①C7H10O4是六元环化合物,②一个碳原子上连两个羟基不稳定,要脱水生成-C-,有下列合成路线。
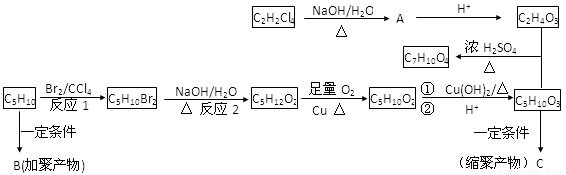
请回答下列问题
(1)反应1的反应类型______________反应2的反应类型___________
(2)C2H4O3分子中所含官能团的名称____________________________
(3)写出B的结构简式_____________________C的结构简式__________________________
(4)C2H2Cl4→A的化学方程式_____________________________________________________
(5)C5H12O2→C5H10O2的化学方程式_______________________________________
(6)C5H10O2的同分异构体中,属于酯类的同分异构体有______种
科目:高中化学 来源:2014-2015四川省达州市高一3月月考化学试卷(解析版) 题型:选择题
在离子RO42—中,共有x个核外电子,R的质量数为A,则R原子核内含有的中子数目为
A.A-x+48 B.A-x+24 C.A-x+34 D.A-x-24
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市西北狼教育联盟高三第二次联合考试理综化学试卷(解析版) 题型:选择题
下列各组热化学方程式中,化学反应的ΔH前者大于后者的是
①C(s)+O2(g)===CO2(g) ΔH1 C(s)+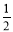 O2(g)===CO(g) ΔH2
O2(g)===CO(g) ΔH2
②S(s)+O2(g)===SO2(g) ΔH3 S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+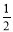 O2(g)===H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
O2(g)===H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)===CaO(s)+CO2(g) ΔH7 CaO(s)+H2O(l)===Ca(OH)2(s) ΔH8
A.①② B.②③ C.②③④ D.①②③
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省高三4月联考理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构基础】(15分)有机反应中常用镍作催化剂。某镍催化剂中含Ni 64.0%、Al 24.3%、Fe 1.4%,其余为C、H、O、N等元素。
(1)氰酸(HOCN)的结构式是 ,其中碳原子的杂化方式是 ,根据等电子体原理,可推测氰酸根离子的空间构型是 。
(2)用Cr2O3作原料,铝粉作还原剂的铝热法是生产金属铬的主要方法之一,该反应是一个自发放热反应,由此可判断Cr-O键和Al-O键中________________键更强。研究发现气态氯化铝(Al2Cl6)是具有配位键的化合物,可溶于非极性溶剂,分子中原子间成键的关系如下图所示。由此可知该分子是 (填“极性”或“非极性”)的。请在图中是配位键的斜线上加上箭头。

(3)铁有α、γ、δ三种晶体构型,其中α-Fe单质为体心立方晶体,δ-Fe单质为简单立方晶体。则这两种晶体结构中铁原子的配位数之比是 ,设α-Fe晶胞边长为a nm,δ-Fe晶胞边长为bnm,则这两种晶体的密度比为 。(用a、b的代数式表示)
(4)氧化镍(NiO )是一种纳米材料,比表面积S(m2/g)是评价纳米材料的重要参数之一(纳米粒子按球形计)。 基态Ni2+有 个未成对电子,已知氧化镍的密度为ρg/cm3;其纳米粒子的直径为Dnm列式表示其比表面积 m2/g。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省高三4月联考理综化学试卷(解析版) 题型:选择题
金属锂燃料电池是一种新型电池,比锂离子电池具有更高的能量密度。它无电时也无需充电,只需更换其中的某些材料即可,其工作示意图如下,下列说法正确的是
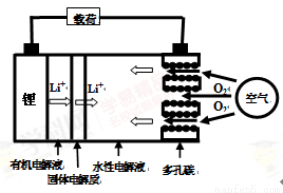
A.放电时,空气极为负极
B.放电时,电池反应为:4Li+O2=2Li2O
C.有机电解液可以是乙醇等无水有机物
D.在更换锂电极的同时,要更换水性电解液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年贵州省八校联盟高三第二次联考理综化学试卷(解析版) 题型:实验题
(14分)某研究性学习小组用下图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
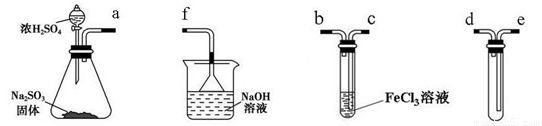
(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在________中,再加水稀释。
(2)组装仪器按气流方向正确的连接顺序是a接____,____接____,____接____。
(3)烧杯中倒置漏斗的作用是______________________________________。
(4)往FeCl3溶液中通入足量SO2时,观察到的现象为_______________________。
(5)根据以上现象,该小组同学认为SO2与FeCl3溶液发生了氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:___________________________;
②请设计实验方案检验有Fe2+生成:__________________________________;
③该小组同学向盛装FeCl3试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法不合理,理由是_________________
查看答案和解析>>
科目:高中化学 来源:2014-2015学年贵州省八校联盟高三第二次联考理综化学试卷(解析版) 题型:选择题
化学知识在生产和生活中有着重要的应用。下列说法中,错误的是
A.家中发生天然气泄漏,不能在室内用电话报警
B.洁厕剂和漂白精不能混合使用,否则易产生有毒气体
C.双氧水可用于杀菌、消毒、漂白
D.明矾既可用于净水,又可杀菌消毒
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高一下学期学期第一次月考化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z,其中X、Z同主族,Y、Z同周期,Z原子最外层电子数是X原子内层电子数的3倍,是Y原子最外层电子数的2倍。下列说法错误的是
A.Y位于第3周期 B.含X、Z的酸不只一种
C.原子半径:Y>Z D.气态氢化物稳定性:Z>X
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省分校高一下学期第一次月考化学试卷(解析版) 题型:选择题
在密闭容器中进行X2(气)+2Y2(气) Z(气)的反应,X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.3mol/L,当反应达到其最大限度(即化学平衡状态)时,各物质的浓度有可能的是
Z(气)的反应,X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.3mol/L,当反应达到其最大限度(即化学平衡状态)时,各物质的浓度有可能的是
A.c(Z)=0.45mol/L
B.c(X2)=0.3mol/L c(Z)=0.1 mol/L
C.c(X2)=0.5mol/L
D.c(Y2)=0.5mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com