

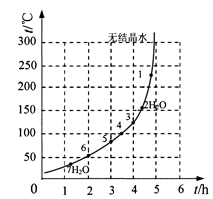
| 序号 | t/h | t/℃ | m/g | x |
| 1 | 3 | 80 | 5 | 4 |
| 2 | 3 | 160 | 10 | 1 |
| 3 | 4 | 160 | 10 | 0.8 |
| 4 | 4 | 160 | 5 | 0 |
| 5 | 5 | 80 | 5 | 3 |
| 6 | 5 | 160 | 15 | 1 |


科目:高中化学 来源:不详 题型:单选题
| A.汽油失火时,立即用水灭火 |
| B.电线短路失火时,可立即用泡沫灭火器灭火 |
| C.浓硫酸溅到皮肤上,立即用稀 NaOH 溶液洗涤 |
| D.浓 NaOH 溶液溅到皮肤上,立即用水冲洗,然后涂上硼酸溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
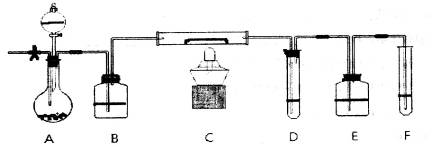
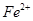 ,如何检验含有Fe2+____________________________________。
,如何检验含有Fe2+____________________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向1 mL 1% NaOH溶液加入2 mL 2%的CuSO4溶液,振荡后滴加0.5 mL葡萄糖溶液,加热 | 未出现红色沉淀 | 葡萄糖中不含有醛基 |
| B | 向溶液X中先滴加盐酸,再滴加BaCl2溶液 | 滴加盐酸时无明显现象,滴加BaCl2溶液时出现白色沉淀 | X中一定含有SO42- |
| C | AgCl饱和溶液中加入少量NaI溶液 | 产生黄色沉淀 | Ksp(AgI)>Ksp(AgCl) |
| D | 向加入了几滴酚酞试液的Na2CO3溶液中滴加BaCl2溶液 | 红色逐渐褪去 | Na2CO3溶液中存在水解平衡 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用过滤法分离氢氧化铁胶体和三氯化铁溶液的混合物 |
| B.将5.85gNaCl固体溶于1000mL容量瓶中,加水定容后即可制得0.1mol?L-1的NaCl溶液 |
| C.向含有少量Ca(OH)2的Mg(OH)2悬浊液中加入饱和MgCl2溶液,充分搅拌后过滤,洗涤,可达到除去Mg(OH)2中的少量Ca(OH)2的目的 |
| D.精炼铜时,粗铜做阴极,纯铜做阳极,电解质溶液为CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实 验 | 现象或结论 |
| A | 取少量某溶液,滴加过量的稀盐酸无明显现象,再滴加BaCl2溶液 | 出现白色沉淀,则该溶液中含有SO42- |
| B | 相同温度下,取两份等质量的锌粒分别与足量稀酸反应,向其中一份中加入几滴CuSO4溶液 | 加入ZnSO4溶液的产生氢气快,最终二者生成氢气的量相同 |
| C | 相同温度下,等质量的大理石与等体积、等浓度的盐酸反应 | 反应速率:粉状大理石>块状大理石 |
| D | 向Na2S溶液中滴入ZnSO4溶液有白色沉淀生成,再加入几滴ZnSO4溶液 | 沉淀由白色转化为黑色,说明溶度积(Ksp):ZnS>CuS |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.燃着的酒精灯不慎碰翻失火,应该迅速用湿抹布扑盖 |
| B.用电子天平称量化学药品时,必须先称小烧杯的质量,再称量加入试剂后的总质量,两者之差即为药品的质量。 |
| C.制备摩尔盐的过程中,洗涤硫酸亚铁铵晶体时,应用少量酒精洗去晶体表面附着的水分 |
| D.在适量氯化钴的乙醇溶液中,逐滴加入水至溶液恰好呈粉红色,加热该溶液,结果依次呈现紫色、蓝紫色、蓝色的变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溴乙烷在浓硫酸作用下加热可制得乙烯. |
| B.在制备乙酸乙酯实验中,长导管有冷凝蒸汽和导气的作用,饱和碳酸钠溶液液面上有油状并有香味液体生成 |
| C.实验室可用无水乙醇和过量的3mol/L硫酸的混合液制乙烯 |
| D.用电石和水可制得纯净的乙炔 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com