
��1��ijѧ������11.9 mol·L-1��Ũ���������ˮ����500 mL���ʵ���Ũ��Ϊ0.400 mol·L-1��ϡ���ᡣ ��ѧ����Ҫ��ȡ________mLŨ����������ơ�������С�����1λ��
��2������ƿ��������Һ�ı������������й�������ƿ����ʹ�÷������������������
��������һ�����ʵ���Ũ�ȵ���Һ��ר������
��ʹ��ǰҪ�ȼ������ƿ�Ƿ�©Һ
������ƿ������������
�ܲ���������ƿ�����������ƺõ���Һ
�ݿ�����500mL����ƿ����250mL��Һ
������ƿ�ϱ��е����¶� ������ ���̶���
a���� �� b���� �� c���� �� d���� ��
��3���� ��ͬѧ�����Ƶ�0.400 mol·L-1�����ᣬ�кͺ�0.4 g NaOH��NaOH��Һ�����ͬѧ��ȡ________mL���ᡣ
�� �����ͬѧ�������Ƶ������кͺ�0.4 g NaOH��NaOH��Һ�����ֱȢ����������ƫС������ܵ�ԭ����________��
a��Ũ����ӷ���Ũ�Ȳ���
b��������Һʱ��δϴ���ձ�
c��������Һʱ����������ƿ�̶���
d����ˮʱ�����̶��ߣ��ý�ͷ�ι�����
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���෨��ѧϰ��ѧ����Ҫ��������������ʶ����ʱ�ɲ��ö��ַ�������±��������
| ��� | ����� | ���� |
| A | FeSO4��NO2��MnO2��NaClO��Cu3P��Na2O2 | H2SO3 |
| B | CH3COOH��HOOC—COOH��HClO��H2S | HF |
| C | ���ֽⷴӦ����ⷴӦ�����ȷ�Ӧ�����ӷ�Ӧ | ��ɫ��Ӧ |
| D | (NH4)2SO4��NH4Cl��NH4NO3��NH3·H2O | NH4HCO3 |
(1)A�з������______________________________________________��H2SO3________(��ǡ���)�ɹ�Ϊ���ࡣ
(2)B�з������_________________________________________________��HF________(��ǡ���)�ɹ�Ϊ���ࡣ
(3)C�з������__________________����ɫ��Ӧ����________�仯��
(4)D�з������__________________��NH4HCO3________(��ǡ���)�ɹ�Ϊ���ࡣ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й��ڻ�ѧƽ�ⳣ��K��˵������ȷ����
A��ƽ�ⳣ���Ĵ�С����ʼŨ���й� B��KֵԽ��,��Ӧ��ת����ԽС
C��KֵԽ��Ӧ��ת����Խ�� D���¶�Խ�ߣ�KֵԽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�輰�仯�����ڲ���������Ӧ�ù㷺������������ȷ����
A���赥�������첣������Ҫԭ��
B��CaSiO3����������̫���ܵ��
C��ˮ�����Ҫ�ɷ���Na2SiO3��CaSiO3��SiO2
D�������������������IJ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и�ѡ������������Ҫ��ȡ�����ʣ������ܹ��õ�����
A��CaCO3  CaO
CaO  Ca(OH)2
Ca(OH)2  NaOH��Һ
NaOH��Һ
B�� Cu CuO
CuO CuSO4��Һ
CuSO4��Һ  Cu(NO3)2��Һ
Cu(NO3)2��Һ
C��KMnO4 O2
O2 SO3
SO3  H2SO4
H2SO4
D ��NH3  NO
NO  NO2
NO2  HNO3
HNO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й����Ƽ��仯�������������ȷ����(����)
A�����ͷ��к���̼�����ƣ���ʹ���Ƴ��ĸ�����ɶ��
B�������ƿ����ں����������Ϊ��������Դ
C��̼���Ƶ�ˮ��Һ������
D������������ʱ�������ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���ǣ��� ��
A��Ԫ�صĵ���һ�����ɻ�ԭ��Ԫ�صĻ��������Ƶ�
B���������Ԫ�صĻ����ﲻһ�����к�ǿ��������
C��������ֻ�ܵõ����ӱ���ԭ��������ֻ��ʧȥ���ӱ�����
D���ڻ�ѧ��Ӧ�У��õ���Խ������������������Ծ�Խǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
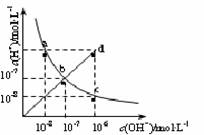
25��ʱ��ˮ��Һ��c(H+)��c(OH��)�ı仯��ϵ��ͼ������a c��ʾ�������жϴ������
A��a c�����ϵ�����һ�㶼��c(H+)·c(OH��)��10-14
B��b d�߶�������һ���Ӧ����Һ��������
C��d���Ӧ��Һ���¶ȸ���25�棬pH��7
D��CH3COONa��Һ������λ��c��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��20.0 g NaOH��ϡ��Һ��ϡ������ȫ��Ӧʱ���ų�28.7 kJ����������ʾ�÷�Ӧ���Ȼ�ѧ����ʽ��ȷ����
A��NaOH(aq)+HCl(aq)��NaCl(aq)+H20(l)  = +28.7 kJ·mol-1
= +28.7 kJ·mol-1
B��NaOH(aq)+HCl(aq)��NaCl(aq)+H20(l)  = -28.7 kJ·mol-1
= -28.7 kJ·mol-1
C��NaOH(aq)+HCl(aq)��NaCl(aq)+H20(l)  = +57.4 kJ·mol-1
= +57.4 kJ·mol-1
D��NaOH(aq)+HCl(aq)��NaCl(aq)+H20(l)  = -57.4 kJ·mol-1
= -57.4 kJ·mol-1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com