
在标准状况下,某烃的密度是1.25 g·L-1,一定体积的该烃完全燃烧生成4.48 L CO2和3.6 g水,求该烃的分子式。
科目:高中化学 来源:2014年高中化学人教版选修四第二章 化学反应速率与化学平衡练习卷(解析版) 题型:选择题
已知反应A(g)+3B(g)=2C(g)+D(g)在某段时间内以A的浓度变化表示的化学反应速率为1 mol/(L·min),则此段时间内以C的浓度变化表示的化学反应速率为( )
A.0.5 mol/(L·min) B.1 mol/(L·min)
C.2 mol/(L·min) D.3 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第一章 化学反应与能量练习卷(解析版) 题型:选择题
充分燃烧一定量的丁烷气体放出的热量为Q。完全吸收它生成的CO2气体生成正盐,需5 mol·L-1的NaOH溶液100 mL,则丁烷的燃烧热为( )
A.16Q B.8Q C.4Q D.2Q
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四模块质量检测练习卷(解析版) 题型:选择题
常温下,pH=11的氨水溶液和pH=1的盐酸溶液等体积混合后(不考虑混合后溶液体积的变化),恰好完全反应,则下列说法不正确的是( )
A.弱碱的浓度大于强酸的浓度
B.反应完全后的溶液呈碱性
C.原氨水中有1%的含氮微粒为NH4+
D.反应后的溶液中NH4+、NH3·H2O与NH3三种微粒的平衡浓度之和为0.05 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四模块质量检测练习卷(解析版) 题型:选择题
氢气是人类最理想的能源。已知在25℃、101 kPa下,1 g 氢气完全燃烧生成液态水时放出热量142.9 kJ,则下列热化学方程式书写正确的是( )
A.2H2+O2=2H2O ΔH=-142.9 kJ·mol-1
B.2H2(g)+O2(g)=2H2O(l)ΔH=-142.9 kJ·mol-1
C.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ·mol-1
D.2H2(g)+O2(g)=2H2O(l)ΔH=+571.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014年甘肃省第二学期第二学段段中考试化学(理科)试卷(解析版) 题型:填空题
(8分)写出下列相应的化学方程式
(1)乙烯→乙醇: (2)丙烯→聚丙烯:
(3)苯→溴苯: (4)苯→环己烷:
查看答案和解析>>
科目:高中化学 来源:2014年7月山东省泰安市高二年级考试化学(物质结构与性质)试卷(解析版) 题型:填空题
(7分)金属及其化合物在生产、生活中有广泛应用。
(1)从结构角度分析Fe3+较Fe2+稳定的原因。
(2)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体属于 晶体。
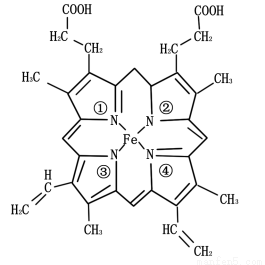
(3)铁元素为血红蛋白和肌红蛋白的活性部分———血红素的重要组成元素,血红素的结构简式如下图所示。与铁原子形成配位键的是 号氮原子(填写氮原子标号)。
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,更适合作录音带磁粉原料的是(填化学式)。
查看答案和解析>>
科目:高中化学 来源:2014年7月山东省泰安市高二年级考试化学(有机化学基础)试卷(解析版) 题型:选择题
现有一瓶乙二醇和丙三醇的混合物,已知它们的性质如下表,据此,将乙二醇和丙三醇互相分离的最佳方法是
物质 | 熔点 | 沸点 | 密度 | 溶解性 |
乙二醇 | -11.5℃ | 198 ℃ | 1.11 g·mL-1 | 易溶于水和乙醇 |
丙三醇 | 17.9 ℃ | 290 ℃ | 1.26 g·mL-1 | 能跟水、酒精以任意比互溶 |
A. 萃取法B. 结晶法C. 分液法D. 蒸馏法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com