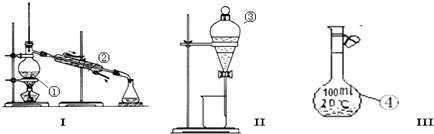
分析:(1)根据常见仪器的名称来回答;
(2)分液漏斗和100mL容量瓶在使用前要检查是否漏水;
(3)萃取利用溶质在不同溶剂中溶解度不同,用一种溶剂把溶质从它与另一溶剂所组成的溶液中提取出来,然后分液;
(4)①根据浓溶液配制稀溶液的步骤选择仪器;
②根据c=
计算浓硫酸的物质的量浓度,根据稀释定律,稀释前后溶质硫酸的物质的量不变,据此计算需要浓硫酸的体积;
③根据c=
判断溶液配制的误差.
解答:解:(1)因①~④仪器的名称分别为:蒸馏烧瓶、冷凝管、分液漏斗、100mL容量瓶,
故答案为:蒸馏烧瓶;冷凝管;分液漏斗;100mL容量瓶;
(2)因分液漏斗和100mL容量瓶在使用前要检查是否漏水,蒸馏烧瓶、冷凝管不需要检查是否漏水,故答案为:③④;
(3)碘在四氯化碳中的溶解度较在水中大,并且四氯化碳和水互不相溶,可用萃取的方法分离,接着可用分液方法将两层液体分开,则选择装置Ⅱ,然后再选择装置I进行蒸馏操作得到单质碘,故答案为:Ⅱ;萃取;分液;I;蒸馏;
(4)①)操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用量筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,
由提供的仪器可知还需要仪器有:100mL容量瓶、胶头滴管,
故答案为:10mL量筒;胶头滴管;100mL容量瓶;
②浓H
2SO
4的物质的量浓度c=
mol/L=18.4mol/L,根据稀释定律,稀释前后溶质硫酸的物质的量不变,设浓硫酸的体积为xL,所以xL×18.4mol/L=0.1LL×0.5mol/L,解得:x≈0.0027L=2.7mL,
故答案为:2.7;
③A.取浓硫酸时俯视,量取硫酸偏少,则配制溶液的浓度偏低,故A不选;
B.将浓硫酸倒出后,洗涤装置,并将洗涤液倒入烧杯中,量筒洗涤后,取硫酸偏大,则配制溶液的浓度偏大,故B选;
C.在烧杯中稀释浓硫酸后,立即转移,温度较高,定容后体积偏小,则配制溶液的浓度偏大,故C选;
D.定容时俯视,体积偏小,则配制溶液的浓度偏大,故D选;
E.颠倒摇匀后发现液面低于刻度线,但未加水至刻度线,无影响,故D不选;
故答案为:BCD.
点评:本题考查混合物的分离、提纯,侧重混合物分离装置及溶液配制的考查,把握装置中仪器的作用及溶液配制的步骤为解答本题的关键,注意根据c=
理解溶液配制原理与误差分析,注意浓硫酸的稀释,仪器选择时规格为解答的易错点,题目难度不大.




 名校课堂系列答案
名校课堂系列答案
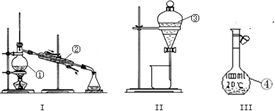 (1)写出图中序号①~④仪器的名称:
(1)写出图中序号①~④仪器的名称: