
| A. | ①②③④⑥ | B. | ①③④⑦⑧ | C. | ③④⑤⑥⑦ | D. | ①②④⑤⑧ |
分析 ①混合物是由多种物质组成的物质;
②能够源源不断的从自然界得到补充的能源叫可再生能源;
③纯净物是由一种物质组成的物质,化合物是由不同种元素组成的纯净物;
④合金是由两种或两种以上的金属与非金属经一定方法所合成的具有金属特性的物质;
⑤食醋的主要成分为乙酸,属于混合物;
⑥纯碱属于盐,熟石灰属于碱;
⑦烟,雾分散质微粒直径在1-100nm;
⑧胶体具有有达尔效应,溶液无此性质;
解答 解:①粗盐含有杂质和酸雨中溶有二氧化硫都是混合物,故①正确;
②沼气是由发酵产生的,属于可再生能源,但水蒸气水高温产生的,则是不可再生能源,故②错误;
③冰和干冰都是由一种物质组成的物质,是纯净物,都是由不同种元素组成的纯净物,又是化合物,故③正确;
④不锈钢和目前流通的硬币都是由两种或两种以上的金属组成的,是合金,故④正确;
⑤硫酸电离阳离子全为氢离子,为酸,属于化合物;食醋是含有醋酸和水,属于混合物,故⑤错误;
⑥纯碱是由钠离子和碳酸根离子组成的化合物,属于盐;熟石灰属于碱,故⑥错误;
⑦烟,雾分散质微粒直径在1-100nm,形成的分散系为胶体,故⑦正确;
⑧胶体具有有达尔效应,溶液无此性质,利用丁达尔效应可以区分溶液和胶体,故⑧正确;
故选:B.
点评 本题考查物质的分类,难度不大,熟悉物质的分类及常见的概念即可解答,平时注意知识的积累.


科目:高中化学 来源: 题型:填空题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
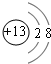 .
.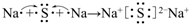 .
.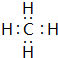 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
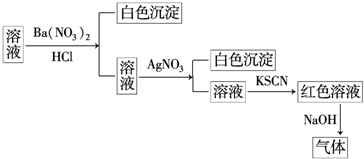
| A. | 原溶液中一定含有SO42- | B. | 原溶液中一定含有NH4+ | ||
| C. | 原溶液中一定含有Cl- | D. | 原溶液中一定含有Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
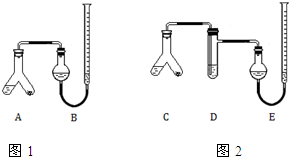 某实验小组分别用图1、2装置测定某种钙片中碳酸钙的含量,夹持装置已略去.
某实验小组分别用图1、2装置测定某种钙片中碳酸钙的含量,夹持装置已略去.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
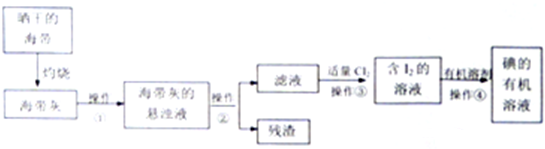
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
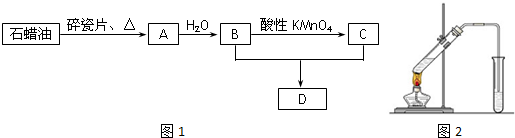
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

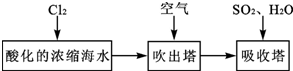
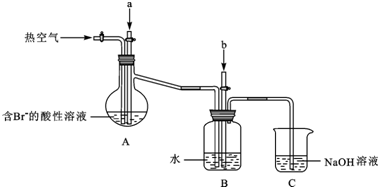
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
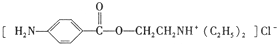 )是一种局部麻醉剂,麻醉作用较快、较强,毒性较低,其合成路线如下:
)是一种局部麻醉剂,麻醉作用较快、较强,毒性较低,其合成路线如下: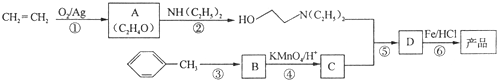
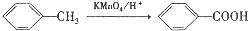
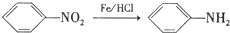
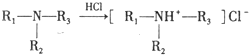
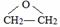 .
.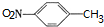 ,C中含氧官能团的名称为硝基、羧基.
,C中含氧官能团的名称为硝基、羧基.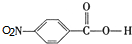 +HOCH2CH2N(C2H5)2 $\stackrel{一定条件下}{→}$
+HOCH2CH2N(C2H5)2 $\stackrel{一定条件下}{→}$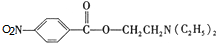 +H2O.
+H2O.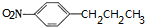 (任写一种).
(任写一种).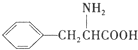 )是人体必需的氨基酸之一,写出其发生缩聚反应的化学方程式
)是人体必需的氨基酸之一,写出其发生缩聚反应的化学方程式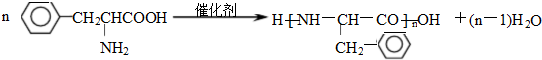 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com