
| A. | 氯化钙的化学式:CaCl | |
| B. | 镁离子结构示意图: | |
| C. | 碳酸钠的电离方程式:Na2CO3═Na++CO32- | |
| D. | 氢氧化钡的电离方程式Ba(OH)2═Ba2++2OH- |
分析 A.化学式是元素符号和小数字组成的表示物质组成的式子,氯化钙中钙为+2价,氯为-1价;
B.镁离子为阳离子,为镁原子失去最外层2个电子形成;
C.电离方程式左右电荷不守恒;
D.氢氧化钡为二元强碱,完全电离出钡离子和氢氧根离子.
解答 解:A.氯化钙中钙为+2价,氯为-1价,化学式为CaCl2,故A错误;
B.镁原子序数为12的元素,质子数为12,镁离子核外电子数为10,有2个电子层,最外层有8个电子,离子结构示意图为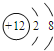 ,故B错误;
,故B错误;
C.碳酸钠的电离方程式为:Na2CO3═2Na++CO32-,故C错误;
D.氢氧化钡为二元强碱,完全电离:Ba(OH)2═Ba2++2OH-,故D正确;
故选D.
点评 本题考查了化学式、离子结构示意图、电离方程式的表示方法判断,题目难度不大,注意掌握常见化学用语的表示方法,明确电离方程式的书写原则.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 此时16O的相对原子质量为32 | |
| B. | 40gNaOH溶于水配成1L溶液,其物质的量浓度为1 mol/L | |
| C. | 标况下44gCO2的体积为22.4L | |
| D. | NA个氧分子与NA个氢分子有相同数目的分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 75%的酒精溶液 | B. | HCl(气态) | C. | Fe (OH)3胶体 | D. | 豆浆 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅧA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
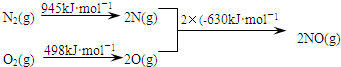
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入水时,平衡向正反应方向移动,溶液中n(H+)增大 | |
| B. | 加入少量冰醋酸,平衡向正反应方向移动,溶液中c(H+)增大 | |
| C. | 加入少量0.1 mol•L-1 HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减小 | |
| D. | 加入少量CH3COONa固体,平衡向逆反应方向移动,溶液中c(H+)减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com