
| A���٢ڢۢ� | B���٢ڢ� |
| C���ڢۢܢݢ� | D��ȫ�� |
| ||


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��48g O3���庬��6.02��1023��O3���� |
| B��5.6g Fe��������ϡ���ᷴӦת�Ƶ���0.3 mol |
| C��0.5mol?L-1CuCl2��Һ�к���3.01��1023��Cu2+ |
| D����״���£�33.6LH2O����9.03��1023��H2O���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������ΪNA��NO2��CO2��������к��е���ԭ����Ϊ2NA |
| B��0.5molO3��11.2LO2�����ķ�����һ����� |
| C��28g��ϩ��C2H4���ͻ����飨C4H8���Ļ�������к��е�̼ԭ����Ϊ2NA |
| D��500mL 1mol/LNa2SO4��Һ�к�Na+��ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��B��ͬ���ڵ�һ��������С��Ԫ�أ�C��������������ɵ����ӣ�E����Χ�����Ų�ʽΪ3d64s2���ش��������⣺
��B��ͬ���ڵ�һ��������С��Ԫ�أ�C��������������ɵ����ӣ�E����Χ�����Ų�ʽΪ3d64s2���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���¡���ѹ |
| ���� |
| 1 |
| 4 |
| 1 |
| 4 |
| 1 |
| 4 |
| 1 |
| 4 |
| 1 |
| 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
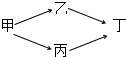 �ס��ҡ��������������ĺ��������������ж�����һ����һ�����ϵĹ����ţ�ͨ������ת����ϵ���ɼ���ȡ������������Է���������Ϊ���������ҵ���Է��������ܴ��ڱ����ش��������⣺
�ס��ҡ��������������ĺ��������������ж�����һ����һ�����ϵĹ����ţ�ͨ������ת����ϵ���ɼ���ȡ������������Է���������Ϊ���������ҵ���Է��������ܴ��ڱ����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼ��ʾ�������̶�������������������ƶ���M��N���������о�������Ӧ��A��g��+3B��g��?2C��g����H=-192kJ?mol-1����M��N�У��ֱ�ͨ��x mol A��y mol B�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䣮����˵����ȷ���ǣ�������
��ͼ��ʾ�������̶�������������������ƶ���M��N���������о�������Ӧ��A��g��+3B��g��?2C��g����H=-192kJ?mol-1����M��N�У��ֱ�ͨ��x mol A��y mol B�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䣮����˵����ȷ���ǣ�������| A����ƽ��ʱA�������������е����������ȣ���xһ������y |
| B����x��y=1��2����ƽ��ʱ��M�е�ת���ʣ�A��B |
| C����x��y=1��3����M�зų�����172.8 kJʱ��A��ת����Ϊ90% |
| D����x=1.4��y=1��N�дﵽƽ��ʱ���Ϊ2L��CΪ0.4mol����Ӧ��ʼʱN�����Ϊ2.6L |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com