
下列叙述中正确的是( )
A. NaHCO3能与碱反应,食品工业用作焙制糕点的膨松剂
B. 工业上制H2SO4过程中SO2氧化条件一般选择高温、高压、催化剂
C. 浓H2SO4有强氧化性,常温下能与Cu发生反应
D. 将C12通入冷的消石灰中可制得漂白粉
考点: 钠的重要化合物;化学平衡的调控作用;氯气的化学性质;浓硫酸的性质.
专题: 元素及其化合物;化学应用.
分析: A.将C12通入冷的消石灰中可制得漂白粉,主要是利用了小苏打的不稳定性;
B.选择在常压下进行;
C.常温下不反应;
D.工业用氯气和石灰乳反应制备漂白粉.
解答: 解:A.将C12通入冷的消石灰中可制得漂白粉,主要是利用了小苏打的不稳定性,反应的方程式为2NaHCO3 Na2CO3+CO2↑+H2O,故A错误;
Na2CO3+CO2↑+H2O,故A错误;
B.常压下转化率已经较大,可选择在常压下进行,故B错误;
C.常温下不反应,应在加热条件下进行,故C错误;
D.工业用氯气和石灰乳反应制备漂白粉,方程式为2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,故D正确.
故选D.
点评: 本题考查钠的重要化合物,侧重于化学与生活的考查,有利于培养学生的良好的科学素养,提高学生学习的积极性,注意相关基础知识的积累,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
在醋酸溶液中,CH3COOH电离达到平衡的标志是( )
|
| A. | 溶液显电中性 |
|
| B. | 溶液中检测不出CH3COOH分子存在 |
|
| C. | 氢离子浓度恒定不变 |
|
| D. | c(H+)=c(CH3COO﹣) |
查看答案和解析>>
科目:高中化学 来源: 题型:
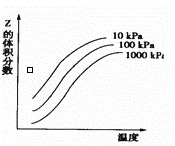
如图表示温度和压强对平衡X+Y⇌2Z的影响.下列叙述正确的是( )
|
| A. | 增大压强,平衡向右移动 |
|
| B. | 升高温度,平衡向左移动 |
|
| C. | X和Y中只有一种为气态,Z为气态 |
|
| D. | 上述反应的正反应为放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 第三周期非金属元素的含氧酸的酸性从左到右依次增强
B. HF、HCl、HBr、HI的热稳定性和还原性从上到下依次减弱
C. 在ⅥA族元素的氢化物(H2R)中,沸点最高的一定是无毒的
D. 同一主族的元素,原子半径越大,其单质的熔点也一定越高
查看答案和解析>>
科目:高中化学 来源: 题型:
W、M、X、Y、Z表示处于三个短周期的五种主族元素,它们的原子序数依次增大,M与X同周期,W与Y同主族,Y与Z同周期,Z在同周期中原子半径最小,M的气态氢化物甲能使湿润的红色石蕊试纸变蓝色,由Y、W、X三种元素组成的物质乙在水溶液中能电离出两种10电子离子.试回答下列各问:(注意:用相应的元素符号、化学式、离子符号表示.)
(1)元素X在周期表中的位置 .
(2)Z的最高价氧化物对应水化物丙的化学式是 ,写出乙与丙反应的离子方程式 .
(3)元素M的单质分子的电子式为 ,物质甲分子的结构式 .
(4)用电子式表示化合物YZ的形成过程 .
(5)写出X与Y形成原子个数比为1:1的物质丁与水反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某澄清、透明的浅黄色溶液中,可能含有下列八种离子:Na+、NH4+、Fe3+、Ba2+、Al3+、SO42﹣、HCO3﹣、I﹣,在设计检验方案前的初步分析中,可确定该溶液中能大量存在的离子最多有( )
A. 4种 B. 5种 C. 6种 D. 7种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质中,不能满足组内任意两种物质间在一定条件下均能发生化学反应的是( )
物质
组别 甲 乙 丙
A Al(OH)3 HCl NaOH
B NH3 O2 H2SO3
C SiO2 NaOH HCl
D SO2 Ca(OH)2 NaHCO3
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
我国材料科学家师昌绪在合金钢、高温合金及材料强度的研究领域作出了杰出贡献,荣获2010年度国家最高科学技术奖.
①合金是生活中常见的材料.某合金具有密度小、强度高的优良性能,常用于制造门窗框架.该合金中含量最高的金属为 (填元素符号).
②铁锈的主要成分是 (填化学式),它是钢铁在潮湿的空气中发生吸氧腐蚀的结果.
③玻璃是一种常用的硅酸盐材料.制备普通玻璃的原料有CaCO3、 和 (填化学式).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com