
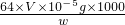 =
=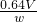 ,
,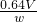 .
.

科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
某含镍(Ni)废催化剂中主要含有Ni,还含有Al、Al2O3、Fe及其他不溶于酸、碱的杂质.部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下:
| 沉淀物 | Al(OH)2 | Fe(OH)3 | Fe(OH))2 | Ni (OH)2 |
| PH | 5.2 | 3.2 | 9.7 | 9.2 |
欲从含镍废催化剂中制得NiSO4?7H2O晶体,其流程如下:
请根据以上信息和流程图,回答下列问题:
(1)“碱浸”的目的是除去含镍废催化剂中的______.
(2)“酸浸”时所加入的酸是_______.酸浸后,滤液②中可能含有的金属离子是______.(用离子符号表示).
(3)“调pH为2-3的目的是______.
(4)步骤A的操作顺序是加热浓缩、冷却、______、______.
(5)NiSO4在强碱溶液中用NaC1O氧化,可制得碱性镍镉电池电极材料NiOOH.该反应的离子方程式为______.
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
| 试剂 | 现象 | 结论 | |
| A | 金属钠 | 有气体产生 | 含羟基或羧基或羟基、羧基 |
| B | 银氨溶液 | 产生银镜 | 含有醛基 |
| C | 碳酸氢钠溶液 | 产生气泡 | 含有羧基 |
| D | 溴水 | 溶液褪色 | 含有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com