

 4NO+6H2O
4NO+6H2O 4NO+6H2O;
4NO+6H2O;

科目:高中化学 来源:不详 题型:单选题
| A.当电池负极消耗mg气体时,电解池阳极同时有mg气体生成 |
| B.电池负极反应式为:O2 + 2H2O + 4e—= 4OH— |
| C.电解后c(Na2CO3)不变,且溶液中有晶体析出 |
| D.电池中c(KOH)不变;电解池中溶液pH变大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.镁作Y电极 |
| B.电池工作时,Na+向负极移动 |
| C.废液的pH大于NaClO溶液的pH |
| D.X电极上发生的反应为ClO-+2H2O-4e-===ClO3-+4H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
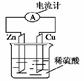
| A.锌片为负极,且逐渐溶解 |
| B.铜片为正极,铜不易失电子而受到保护 |
| C.电子由锌片通过导线流向铜片,H+往铜片运动 |
| D.该装置能将电能转变为化学能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

 (aq)
(aq) PbCO3(s)+SO42-(aq)
PbCO3(s)+SO42-(aq) )=c(SO42-)
)=c(SO42-)
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
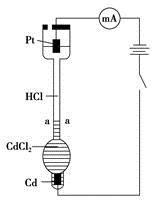
| A.通电后,可观察到清晰界面缓缓向上移动的原因是Cd2+向Pt电极迁移的结果 |
| B.装置中Pt电极附近的pH增大 |
| C.一定时间内,如果通过HCl溶液某一界面的总电量为5.0 C,测得H+所迁移的电量为4.1 C,说明该HCl溶液中H+的迁移速率约是Cl-的4.6倍 |
| D.如果电源正负极反接,则下端产生大量Cl2,使界面不再清晰,实验失败 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
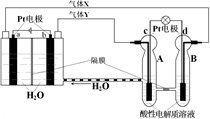
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解池的阳极上发生氧化反应,阴极上发生还原反应 |
| B.原电池的正极上发生氧化反应,负极上发生还原反应 |
| C.电镀时,电镀池里的阳极材料发生氧化反应 |
| D.用原电池作电源进行电解时,电子从原电池负极流向电解池阴极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com