
| 仪器 | 加入试剂 | 预期实验现象 |
| A | 绿矾试样 | ______ |
| B | ______ | ______ |
| D | ______ | ______ |
 Fe2O3+SO2↑+SO3↑+14H2O,
Fe2O3+SO2↑+SO3↑+14H2O, Fe2O3+SO2↑+SO3↑+14H2O.
Fe2O3+SO2↑+SO3↑+14H2O.

科目:高中化学 来源: 题型:阅读理解

| 仪器 | 加入试剂 | 预期实验现象 |
| A | 绿矾试样 | 残留红棕色固体 残留红棕色固体 |
| B | 无水硫酸铜 无水硫酸铜 |
白色粉末变蓝 白色粉末变蓝 |
| D | 品红或酸性高锰酸钾溶液或溴水 品红或酸性高锰酸钾溶液或溴水 |
溶液褪色 溶液褪色 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)资料表明,在加热条件下,三氧化硫具有比较强的氧化性。??
甲同学认为,绿矾受热分解的产物是FeO、SO3、H2O。你支持甲同学的观点吗? (填“支持”或“不支持”)。说明你的理由: 。?
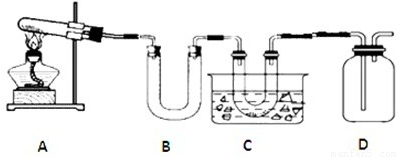
(2)实验是解决问题的重要手段。乙同学用下图装置通过实验来探究绿矾受热分解的产物情况(加热及夹持装置未画出):??

实验过程中发现:装置A中有残留固体,装置B中无水硫酸铜变蓝,装置C中的U形管中有无色晶体出现。?
回答下列问题:?
①在装置C导管出口处还应有的实验现象是 。?
②装置A中残留的固体是 ,装置C中的U形管中无色晶体是 。?
③乙同学为了验证绿矾受热分解的所有产物,在C装置后连接了一个装置,并选用了合适的药品,不仅达到了实验目的而且还起到了一举两得的效果。请你在C装置后的方框中画出该装置,并注明选用的药品。?
④写出绿矾受热分解的化学方程式:?
。?
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:实验题
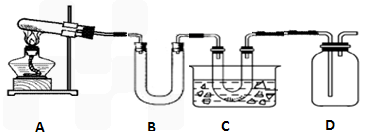

查看答案和解析>>
科目:高中化学 来源:江西省模拟题 题型:实验题
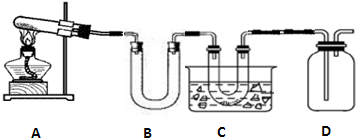

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com