
�ڲ�ͬŨ�ȣ�c)���¶ȣ�T)�����£�����ˮ���˲ʱ���ʣ�v�����±��������жϲ���ȷ���ǣ� ��
|
| 0.600 | 0.500 | 0.400 | 0.300 |
| 318.2 | 3.60 | 3.00 | 2.40 | 1.80 |
| 328.2 | 9.00 | 7.50 | a | 4.50 |
| b | 2.16 | 1.80 | 1.44 | 1.08 |
A��a=6.00 B��ͬʱ�ı䷴Ӧ�¶Ⱥ����ǵ�Ũ�ȣ�v���ܲ���
C��b��318.2 D����ͬ�¶�ʱ������Ũ�ȼ���һ�������ʱ����ͬ
���𰸡�D
��������A.���ݱ�������ݿ�֪���¶Ȳ���ʱ�����ǵ�Ũ��Խ��ˮ�������Խ�졣����Ũ�������ʵı仯��ϵ��֪����328.2Tʱ�����ǵ�Ũ��ÿ��С0.100mol/L��ˮ�����ʼ�С1.50mmol/(L∙min)���������¶���328.2T��Ũ����0.400mol/Lʱ��ˮ���������a=7.50-1.50=6.00 mmol/(L∙min)����ȷ��B�����ݱ������ݿ�֪�������¶ȣ�ˮ��������������Ũ�ȣ�ˮ������Ҳ������ͬʱ�ı䷴Ӧ���Ũ�Ⱥͷ�Ӧ���¶ȣ�����߶�ˮ�ⷴӦ���ʵ�Ӱ�����ؿ����������ʹ��Ӧ���ʿ��ܲ������ı䣬��ȷ��C�������ʵ�Ũ�Ȳ���ʱ�������¶ȣ�ˮ�������������¶ȣ�ˮ�����ʼ�С�����������ʵ�Ũ����0.600mol/Lʱ���¶���318.2Tʱˮ��������3.60 mmol/(L∙min)�����ڸ÷�Ӧ��������2.16 mmol/(L∙min)<3.60 mmol/(L∙min)��˵����Ӧ�¶ȵ���318.2 T����b��318.2����ȷ��D����ͬ�¶�ʱ������Ũ�ȼ��٣��������ʼ����������¶Ȳ�ͬ������ͬ��Ũ��ʱ�ķ�Ӧ���ʲ���ͬ������
�����㶨λ����������ˮ����������¶ȡ����ʵ�Ũ�ȵĹ�ϵ�ļ������жϵ�֪ʶ��
����ʦ�㾦���о���ѧ��Ӧ����Ҫ����Ӧ���еĿ�����ҲҪ������ת���ij̶ȴ�С��������ջ�ѧ��Ӧ���ʡ���ѧƽ���ƶ�ԭ������������ķdz���Ҫ������֪ʶ�����������ǵ�ˮ�ⷴӦΪ�������������¶ȡ�Ũ�ȶ�ˮ�ⷴӦ���ʴ�СӰ�죬ͬʱ����ѧ�������ݽ��й۲졢�������жϺ�Ӧ�õ����������ո������أ��������Ի�ѧ��Ӧ���ʵ�Ӱ�졢�۲����ݵı仯�ص��DZ������Ĺؼ���


 ��ʱѵ���������������ϵ�д�
��ʱѵ���������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�л���A��C��H��O����Ԫ����ɣ���Է�������Ϊ90����9.0 g A��ȫȼ�յIJ�������ͨ��������Ũ����ͼ�ʯ�ң��ֱ�����5.4 g��13.2 g��A����NaHCO3��Һ������Ӧ����2����A֮����ˮ��������Ԫ��������й�A��˵����ȷ����(����)
A������ʽ��C3H8O3
B��A�������IJ����ܷ���������Ӧ
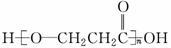 C��0.1 mol A������Na��Ӧ����2.24 L H2(��״��)
C��0.1 mol A������Na��Ӧ����2.24 L H2(��״��)
D��A��һ�������·������۷�Ӧ�IJ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ܱ������У�����2molA��1molB�������·�Ӧ��2A(g)+B(?) 2C(g)+D(g)��
2C(g)+D(g)��
C�����������C%) ��ʱ��ı仯���Ʒ�����ͼ��ϵ��
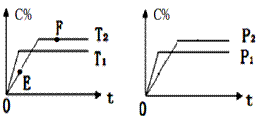
����˵����ȷ����
A��E���v(��)����F���v(��)
B�������������ȣ��÷�Ӧ��ƽ�ⳣ��K������
C������F��ʱ��������ѹ������ƽ��ʱC��Ũ�Ƚ�����
D���ں��º����´�ƽ������������ټ���2molA��1molB��A��ת���ʽ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���ǣ� ��
A����H2O2�ֽ����1molO2,������ת�Ƶĵ�����ԼΪ4��6��02��1023
B�������£�pH=3��CH3COOH��Һ��pH=11��NaOH��Һ�������ϣ���ҺpH>7
C������ˮբ����������������ӵ�����������������ֹ�丯ʴ
D��һ�������·�ӦN2��3H2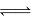 2NH3�ﵽƽ��ʱ��3v��(H2)=2v��(NH3)
2NH3�ﵽƽ��ʱ��3v��(H2)=2v��(NH3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�⼰�仯�����ںϳ�ɱ������ҩ��ȷ�����й㷺��;���ش��������⣺
��1�������ĵ⸻���ں����У���ˮ��ȡ��Ũ��������Ũ��Һ�м�MnO2��H2SO4�����ɵõ�I2���÷�Ӧ�Ļ�ԭ����Ϊ____________��
��2������Ũ��Һ�к���I-��Cl-�����ӣ�ȡһ������Ũ��Һ�������еμ�AgNO3��Һ����AgCl��ʼ����ʱ����Һ��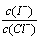 Ϊ��_____________����֪Ksp��AgCl��=1.8��10-10��Ksp��AgI��=8.5��10-17��
Ϊ��_____________����֪Ksp��AgCl��=1.8��10-10��Ksp��AgI��=8.5��10-17��
��3����֪��Ӧ2HI(g) ===H2(g) + I2(g)�Ħ�H= +11kJ��mol��1��1mol H2(g)��1mol I2(g)�����л�ѧ������ʱ�ֱ���Ҫ����436kJ��151kJ����������1molHI(g)�����л�ѧ������ʱ�����յ�����Ϊ______________kJ��
��4��Bodensteins�о������з�Ӧ��
2HI(g) H2(g) + I2(g)
H2(g) + I2(g)
��716Kʱ�����������е⻯������ʵ�������x(HI)�뷴Ӧʱ��t�Ĺ�ϵ���±���
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
�� ��������ʵ�������÷�Ӧ��ƽ�ⳣ��K�ļ���ʽΪ��___________��
�� ������Ӧ�У�����Ӧ����Ϊv��= k����x2(HI)���淴Ӧ����Ϊv��=k����x(H2)��x(I2)������k����k��Ϊ���ʳ�������k��Ϊ________(��K��k����ʾ)����k�� = 0.0027min-1����t=40minʱ��v��=__________min-1
�� ������ʵ�����ݼ���õ�v��~x(HI)��v��~x(H2)�Ĺ�ϵ������ͼ��ʾ�������ߵ�ijһ�¶�ʱ����Ӧ�� �´ﵽƽ�⣬��Ӧ�ĵ�ֱ�Ϊ_________________������ĸ��
�´ﵽƽ�⣬��Ӧ�ĵ�ֱ�Ϊ_________________������ĸ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���Ǻϳ����ᡢ��κ͵��ʵĻ���ԭ�ϣ��ش��������⣺
��1������ˮ��Һ�������ԣ���ԭ��Ϊ �������ӷ���ʽ��ʾ����0��1 mol��L-1�İ�ˮ�м���������NH4Cl���壬��Һ��PH ������ߡ����͡�������������������������Һ�е�NH4+��Ũ�� �������С������
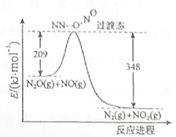 ��2������識��ȷֽ�ɵõ�N2O��H2O��250��ʱ����������ܱ������зֽ�ﵽƽ�⣬�÷ֽⷴӦ�Ļ�ѧ����ʽΪ ��ƽ�ⳣ������ʽΪ ������1mol�������ȫ�ֽ⣬ת�Ƶĵ�����Ϊ mol��
��2������識��ȷֽ�ɵõ�N2O��H2O��250��ʱ����������ܱ������зֽ�ﵽƽ�⣬�÷ֽⷴӦ�Ļ�ѧ����ʽΪ ��ƽ�ⳣ������ʽΪ ������1mol�������ȫ�ֽ⣬ת�Ƶĵ�����Ϊ mol��
��3����N2O��NO��Ӧ����N2��NO2�������仯��ͼ��ʾ��������1molN2�� ���H= kJ��mol-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ҹ��Ŵ���ͭ�����վ�տ���кܸߵ�������ֵ����ʷ��ֵ������������ͭ������ܵ�������ʴ���ʶ���������ͷ���������Ҫ���塣
��1��ԭ������Ϊ29��ͭԪ��λ��Ԫ�����ڱ��е� ���ڡ�
��2��ij��ͭ����Sn��Pb�������ֱ�Ϊ119g��20.7g�������ͭ����Sn��Pbԭ�ӵ���Ŀ֮��Ϊ ��
��3���о����֣���ʴ���ص���ͭ���������CuCl������CuCl����ͭ����ʴ�����еĴ����ã�����������ȷ���� ��
A�������˷�Ӧ�Ļ�� B�������˷�Ӧ������
C�������˷�Ӧ���ʱ� D�������˷�Ӧ��ƽ�ⳣ��
��4�����á��ֲ���շ������Է�ֹ��ͭ����һ������ʴ���罫��״Ag2OͿ�ڱ���ʴ��λ��Ag2O���к����CuCl�������ֽⷴӦ���û�ѧ����ʽΪ ��
��5����11ͼΪ��ͭ���ڳ�ʪ�����з����绯ѧ��ʴ��ԭ��ʾ��ͼ��
�ٸ�ʴ�����У������� ����ͼ����ĸ��a����b����c������
�ڻ����е�Cl-��ɢ���ڣ�����������Ӧ���������Ӧ�����������ɶ��״��u2(OH)3Cl�������ӷ���ʽΪ ��
��������4.29 g Cu2(OH)3Cl���������Ϻ������Ϊ L����״������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1L 1.0mol•L��1 NaOH��Һ����0.8mol CO2��������Һ�е�CO32����HCO3����Ũ��֮��Լ�ǣ���
| A�� | 1��3 | B�� | 1��2 | C�� | 2��3 | D�� | 3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��O2��HClת��ΪCl2�������Ч�棬������Ⱦ��
��1����ͳ�ϸ�ת��ͨ������ͼ��ʾ�Ĵ���ѭ��ʵ�֣�
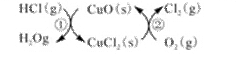
���У���Ӧ��Ϊ��2HCl(g) + CuO(s) 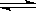 H2O(g)+CuCl2(g) ��H1
H2O(g)+CuCl2(g) ��H1
��Ӧ������1molCl2(g)�ķ�Ӧ��Ϊ��H2�����ܷ�Ӧ���Ȼ�ѧ����ʽΪ , (��Ӧ���á�H1�͡�H2��ʾ)��
��2������RuO2����������HClת��ΪCl2���ܷ�Ӧ���и��õĴ� �����ԣ�
�����ԣ�
��ʵ������һ��ѹǿ�£��ܷ�Ӧ��HClƽ��ת�������¶ȱ仯��aHCl��T������ͼ12�����ܷ�Ӧ�ġ�H 0 ,�����������������������A��B�����ƽ�ⳣ��K(A)��K(B)�нϴ���� ��
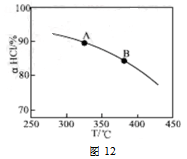
��������ʵ������ѹ�����ʹѹǿ��������ӦaHCl��T���ߵ�ʾ��ͼ������Ҫ˵�����ɣ� ��
�����д�ʩ�����������aHCl���� ��
A������n(HCl) B������n(O2) C��ʹ�ø��õĴ��� D����ȥH2O
��3��һ�������²�÷�Ӧ������n(Cl2)���������£�
| t(min) | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
����2.0��6.0min����HCl�����ʵ����仯��ʾ�ķ�Ӧ���ʣ���mol��min-1Ϊ��λ��д��������̣���
��4��Cl2��;�㷺��д����Cl2�Ʊ�Ư�۵Ļ�ѧ����ʽ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com