
| A、单质的熔点和沸点随核电荷数的增加逐渐升高 |
| B、单质的氧化性随核电荷数的增加逐渐减弱 |
| C、氢化物的稳定性随核电荷数的增加逐渐增强 |
| D、卤素阴离子的还原性随核电荷数的增加逐渐增强 |


科目:高中化学 来源: 题型:

| A、1种 加聚反应 |
| B、2种 缩聚反应 |
| C、3种 加聚反应 |
| D、3种 缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
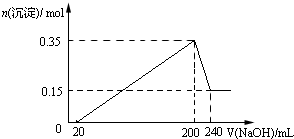 将一定质量的Mg和Al混合物投入到200mL稀硫酸中,固体全部溶解后,向所得溶液中滴加NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法不正确的是( )
将一定质量的Mg和Al混合物投入到200mL稀硫酸中,固体全部溶解后,向所得溶液中滴加NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法不正确的是( )| A、Mg和Al的总质量为9g |
| B、最初20mLNaOH溶液用于中和过量的稀硫酸 |
| C、NaOH溶液物质的量浓度为5mol?L-1 |
| D、生成的氢气在标准状况下的体积为11.2L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b |
| B、若1mL pH=1的盐酸与100mLNaOH溶液混合后,溶液的pH=7则NaOH溶液的pH=11 |
| C、1.0×10-3mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH=8.0 |
| D、在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg2+、OH-、SO42- |
| B、Ag+、Al3+、Cl- |
| C、Cu2+、Cl-、SO42- |
| D、Fe3+、NH4+、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水既是氧化剂又是溶剂 |
| B、总反应为:2Li+2H2O=2LiOH+H2↑ |
| C、放电时正极上有氢气生成 |
| D、放电时OH-向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、麦芽糖及其水解产物均能发生银镜反应 |
| B、用溴水即可鉴别苯酚溶液、2,4-己二烯和甲苯 |
| C、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
D、用甘氨酸(H2N-CH2-COOH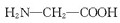 )和丙氨酸( )和丙氨酸(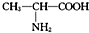 )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na产生的多 |
| B、Mg产生的多 |
| C、Al产生的多 |
| D、一样多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com