
����Ŀ��Cu�ĵ��ʺͺϽ���������������Ź㷺��Ӧ�á��ش��������⣺
(1)Cu�Ļ�̬ԭ�Ӽ۵����Ų�ʽΪ___��
(2)����ͭ�����백ˮ����������ⶼ���ܷ�Ӧ�������백ˮ��������Ļ����Һ��Ӧ����ԭ����___����Ӧ�Ļ�ѧ����ʽΪ___��
(3)������Cu(CN)32-�У��������ӵ��ӻ�������___���������ӵĿռ乹��Ϊ___��CN-����λԭ����___(������)��
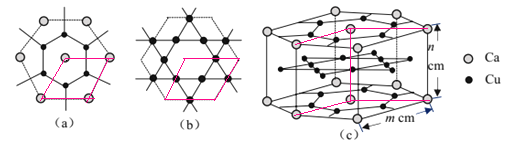
(4)CaCux�Ͻ�ɿ�������ͼ��ʾ��(a)��(b)����ԭ�Ӳ㽻��ѻ����ж��ɡ�(a)����Cu��Ca��ͬ��ɵIJ㣬����Cu��Cu֮����ʵ��������(b)����ȫ��Cuԭ����ɵIJ㣬Cu��Cu֮��Ҳ��ʵ��������ͼ�����߹����������Σ���ʾ�������ֲ�ƽ�жѻ�ʱ��ֱ�ڲ�����λ�ã�(c)����(a)��(b)����ԭ�Ӳ㽻��ѻ���CaCux�Ͻ�ľ���ṹͼ�������ֽṹ�У�ͬһ���Ca��Cu����Ϊ294pm�����������Ca��Cu����Ϊ327pm��
�ٸþ�����Ca��___��Cuԭ����λ(��һ��Ҫ�Ⱦ����)��
��ͬһ���У�Caԭ��֮�����̾�����___pm����NAΪ�����ӵ�������ֵ��CaCu������ܶ���___g/cm3(�ú�m��n��ʽ�ӱ�ʾ)��

���𰸡�3d104s1 ��������Ϊ������������Cu2+�γ������ӣ����߹�ͬ���ô�ʹ��Ӧ���� Cu+H2O2+4NH3=Cu(NH3)4(OH)2 sp2 ƽ�������� ̼ 18 ![]()
![]()
��������
(1)���ݹ���ԭ��������
(2)Cu���л�ԭ�ԣ�H2O2���������ԣ����߷�Ӧ������Cu2+���백ˮ����γ������ӣ�
(3)������������Cu+��ϵ������ӵ���λ��ȷ�����ӻ����ͼ������ӵĿռ乹�ͣ������������ԭ�ӽṹȷ����λԭ�ӣ�
(4)������a��b�㽻��ѻ����ж��ɣ�����ԭ�ӵ����λ�÷����ж���Caԭ����λ��Cuԭ�Ӹ���������������λ�ü������ܶȼ��㹫ʽ���㾧���ܶȡ�
(1)Cu��29��Ԫ�أ���������Ų�ʽ��1s22s22p63s23p63d104s1����̬ԭ�Ӽ۵����Ų�ʽΪ3d104s1��
(2)H2O2����ǿ�������ԣ����Խ����л�ԭ�Ե�Cu����ΪCu2+������Cu2+�γ������ӣ����߹�ͬ���ô�ʹ��Ӧ���У���Ӧ�Ļ�ѧ����ʽΪCu+H2O2+4NH3=Cu(NH3)4(OH)2��
(3)��Cu(CN)32-�У���������Cu+���ӻ�������sp2�ӻ������Ŀռ乹����ƽ�������Σ�������λ��CN-�е�Cԭ��������Cu+��ϣ�����CN-����λԭ����̼ԭ�ӣ�
(4)�ٸ�Ca-Cu������a��b�㽻��ѻ����ж��ɣ���a����Caԭ����Χ��6��Cuԭ�ӣ���b��Caԭ����Χ��12��Cuԭ�ӣ����Ըþ�����Ca��6+12=18��Cuԭ����λ��
�ھ���cΪƽ�������壬a��ͨ��4�����ڵ�Caԭ�ӵ�ƽ���ı���Ϊ���棬b��ƽ���ı���Ϊ������b�������
��֪�����ڲ�1��Cuԭ�ӣ�����Cuԭ��λ�����ϣ�������Cuԭ����ĿΪ1+![]() ��8=5��ͼa����ͼ��ʾ����������
��8=5��ͼa����ͼ��ʾ����������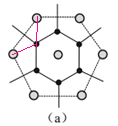 �����Ϊ30����ͬ������Ca-Ca�ľ���Ϊ2��
�����Ϊ30����ͬ������Ca-Ca�ľ���Ϊ2��![]() ��294pm=
��294pm=![]() pm��
pm��
��1�������к��е�Caԭ����ĿΪ��6��![]() +1=3�����е�Cuԭ�Ӹ���Ϊ��6+6+6��
+1=3�����е�Cuԭ�Ӹ���Ϊ��6+6+6��![]() =15�����������V=6��
=15�����������V=6��![]() m2n cm3=
m2n cm3=![]() m2n cm3�������ܶ�
m2n cm3�������ܶ�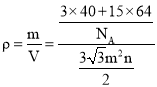 g/cm3=
g/cm3=![]() g/cm3��
g/cm3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ѧ֪ʶ�ش��������⣺
(1)ͬ��ͬѹ�£�H2(g)��Cl2(g)��2HCl(g)���ڹ��պ͵�ȼ�����µġ�H(��ѧ��������ͬ)�ֱ�Ϊ��H1����H2����H1_______��H2(����������������������������ͬ)��
(2)��֪����ʱ���ױȰ����ȶ����Ƚ����з�Ӧ�С�H�Ĵ�С����H1_______��H2��
��P4(���ף�s)��5O2(g)��2P2O5(s) ��H1
��4P(���ף�s)��5O2(g)��2P2O5(s) ��H2
(3)��֪��ϡ��Һ�У�H��(aq)��OH��(aq)��H2O(l) ��H����57.3 kJ��mol��1����Ũ������ϡ����������Һ��Ӧ����1 molˮ���ų�������__________57.3kJ��
(4)��֪��0.5 mol CH4(g)��0.5 molˮ������t�桢pkPaʱ����ȫ��Ӧ����CO��H2�Ļ�����壬������a kJ�������÷�Ӧ���Ȼ�ѧ����ʽ��___________________________________��
(5)������һ����Ҫ�����ʣ���������ȡ���ʺ�����ȡ���֪H��H����N��H����N��N���ļ��ֱܷ���436 kJ��mol��1��391 kJ��mol��1��946 kJ��mol��1��д���ϳɰ����ȷ�Ӧ����ʽ��___________________________________������1 mol NH3��Ҫ���ջ�ų�________kJ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�ͭ���壨CuCl2��2H2O���к���FeCl2���ʣ�Ϊ�Ƶô������Ȼ�ͭ���壬���Ƚ����Ƴ�ˮ��Һ���ٰ���ͼ��ʾ�IJ�����������ᴿ��
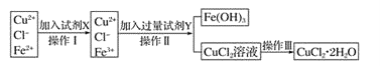
������±�������������ա�

��1������I����X��Ŀ����___________________________ ��
��2���������ʶ�������ΪX���ʺϱ�ʵ���X���ʿ�����_________������ĸ����
A KMnO4 B NaClO C H2O2 D Cl2
��3������II��Y�Լ�Ϊ____________���ѧʽ������������Һ��pH��______��Χ��
��4��ʵ����������CuCl2��Һʱ���������_________�����������ƣ��������ǣ��������������й����ӷ���ʽ��ʾ��__________________________________________��
��5������CuCl2��Һ�������գ��õ��Ĺ�����_________________���ѧʽ������Ҫ����ˮCuCl2���������������______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�����̼����MCO3(M��Mg2����Ca2����Mn��)�ij����ܽ�ƽ��������ͼ��ʾ������˵��������ǣ� ��
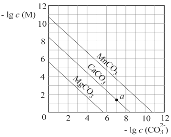
A. Ksp(MnCO3)��������Ϊ10��11
B. MgCO3������Һ�м�������ˮ�����c(Mg2��)����
C. ��Ũ�Ⱦ�Ϊ0.01mol��L��1��Mg2����Ca2����Mn2�������Һ����μ���Na2CO3��Һ�������γ�MgCO3����
D. a���ʾ����Һ�У�c(Ca2��)��c(CO32��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���10mL0.10 mol/L CuCl2��Һ�еμ�0.10mol/L Na2S��Һ���μӹ����У�lgc(Cu2+)��Na2S��Һ���(V)�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����

A. Ksp(CuS)��������Ϊ10��21
B. ������a����Һ�У�c(S2��)c(Cu2+) > Ksp(CuS)
C. a��b��c������Һ�У�n(H+)��n(OH��)�Ļ���С��Ϊb��
D. c����Һ�У�c(Na+)>c(Cl��)>c(S2��)>c(OH��)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У�������������ԭ��Ӧ����
A.2H2O2 ![]() 2H2O + O2��B.NH4Cl
2H2O + O2��B.NH4Cl![]() NH3�� + HCl��
NH3�� + HCl��
C.2Al + Fe2O3![]() 2Fe + Al2O3D.Cu + 2H2SO4(Ũ)
2Fe + Al2O3D.Cu + 2H2SO4(Ũ) ![]() CuSO4 + SO2�� + 2H2O
CuSO4 + SO2�� + 2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�о���AgNO3��Һ�������Һ�е�Cl-��CrO42-�������룬������25��ʱAgCl��Ag2CrO4�������ܻ�������ܽ�ƽ�����ߡ����У�pAg+= -lgc(Ag+)�������������ơ������ཻ���ܽ�ƽ�����߰�ͼ��ֳ���X��Y��Z��M�ĸ���������˵���������( )

A.Ksp(Ag2CrO4)ԼΪ1 ��10-12��Ksp(AgCl)��������Ϊ10-10
B.M�����ڿ�����Ag2CrO4��������������AgCl����
C.��Cl-��CrO42-��Ϊ0.1 mol/ L�Ļ����Һ����μ���ϡ��������Һ��������AgCl����
D.��Ag2CrO4��AgCl��Ϲ����ˮ���ܽ�ƽ����ϵ�м�������ˮ�� ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��¡�1L�ܱ������У�3��������ʼ״̬��ƽ��״̬ʱ�����ʵ�����n�����±���ʾ�������й�˵����ȷ����
x | y | w | |
n(��ʼ)��mol | 2 | l | 0 |
n(ƽ��)��mol | l | 0.5 | 1.5 |
A. ���¶��£��˷�Ӧ��ƽ�ⳣ������ʽ��![]()
B. �����¶ȣ���w�����������С����˷�Ӧ��H>0
C. ����ѹǿ�������淴Ӧ���ʾ�����ƽ��������Ӧ�����ƶ�
D. ���¶��£�����������ͨ��3molw���ﵽƽ��ʱ��n(x)=2mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1mol��L��1MgSO4��0.05mol��L��1Al2(SO4)3��Һ����ʵ�飺����ȡ25mL���ֱ�μ�0.5mol��L��1NaOH��Һ�������ҺpH��V(NaOH)�Ĺ�ϵ��ͼ1������������Һ�������Ϻ�ȡ��25mL����μ�������NaOH��Һ���۲�����������ȷ���� (����)
ͼ1  ͼ2
ͼ2
A.ͼ1�е�����II��ʾMgSO4��NaOH��Ӧ�Ĺ�ϵ
B.����ͼ1�ɵ�Ksp[Al(OH)3]��ֵ����1.0��10��32
C.ʵ������Al(OH)3��ȫ�ܽ�ǰ����Һ��c(Mg2+)/c(Al3+)���
D.ͼ2���Ա�ʾʵ������n(����)��V(NaOH)�Ĺ�ϵ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com