
| A.上述反应中,每消耗2mol NO2,就会生成22.4L N2O |
| B.N2O有氧化性,且为HNO2的酸酐 |
| C.等质量的N2O和CO2含有相等的电子数 |
| D.N2O会迅速与人体血红蛋白结合,使人中毒 |
科目:高中化学 来源:不详 题型:填空题
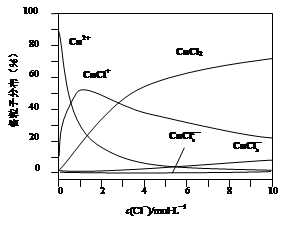
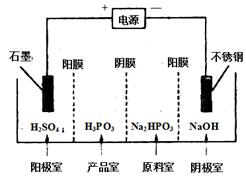
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.8 mol | B.1.1 mol | C.1.2 mol | D.2.0 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应过程中,电子转移数为2NA |
| B.固体生成物的质量为106 g |
| C.CO可能有剩余 |
| D.反应后一定生成11.2 L氧气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.4 mol | B.0.6 mol |
| C.0.8 mol | D.0.2 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氧化产物为Cl2 |
| B.参加反应的氧化剂与还原剂的物质的量之比为1∶2 |
| C.若有3 mol H2O生成,则反应中有2 mol电子转移 |
| D.当该反应生成2.24 L Cl2(标准状况)时,反应中有0.1 mol电子转移 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.8.64 g | B.9.20 g |
| C.9.00 g | D.9.44 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
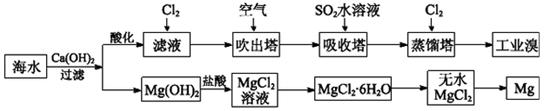
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com