
����Ŀ������(M)���������(��ͼ)����ԭ���á������ܶȸߵ��ŵ㣬������Ϊ����Դ�������ƶ��豸�ĵ�Դ�������طŵ���ܷ�Ӧ����ʽΪ��4M+nO2+2nH2O=4M(OH)n����֪����ص������۱�������ָ��λ�����ĵ缫�������������ͷų��������ܡ�����˵������ȷ����
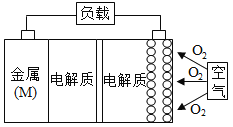
A�����ö�缫��Ŀ������ߵ缫��������Һ�ĽӴ��������������������ɢ���缫����
B���Ƚ�Mg��Al��Zn���ֽ�����������أ�Al��������ص����۱��������
C��M��������طŵ���̵�������Ӧʽ��4Mn++nO2+2nH2O+4ne��=4M(OH)n
D����M����������У�Ϊ��ֹ����������Mg(OH)2���˲������Ե���ʼ������ӽ���Ĥ
���𰸡�C
��������
���������A����Ӧ��Ӵ����Խ��Ӧ����Խ�죬���Բ��ö�缫��Ŀ������ߵ缫��������Һ�ĽӴ��������������������ɢ���缫���棬�Ӷ���߷�Ӧ���ʣ���A��ȷ��B����ص������۱�������ָ��λ�����ĵ缫�������������ͷų��������ܣ���λ�����ĵ缫����ʧȥ���ӵ����ʵ���Խ����õ��ĵ���Խ�࣬������������1gʱ�������ֽ���ת�Ƶ������ʵ����ֱ�Ϊ![]() ��2=
��2=![]() mol��
mol��![]() ��3=
��3=![]() mol��
mol��![]() ��2=
��2=![]() mol������Al-������ص����۱�������ߣ���B��ȷ��C�������������õ��Ӻ�ˮ��Ӧ����OH-����Ϊ�������ӽ���Ĥ�����������Ӳ��ܽ�������������������ӦʽΪO2+2H2O+4e-=4OH-����C����D��������Mgʧ��������Mg2+��Ϊ��ֹ����������Mg(OH)2������������Һ���ܺ��д���OH-�������˲������Ե���ʼ������ӽ���Ĥ����D��ȷ����ѡC��
mol������Al-������ص����۱�������ߣ���B��ȷ��C�������������õ��Ӻ�ˮ��Ӧ����OH-����Ϊ�������ӽ���Ĥ�����������Ӳ��ܽ�������������������ӦʽΪO2+2H2O+4e-=4OH-����C����D��������Mgʧ��������Mg2+��Ϊ��ֹ����������Mg(OH)2������������Һ���ܺ��д���OH-�������˲������Ե���ʼ������ӽ���Ĥ����D��ȷ����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������е�ijЩ���ⳣ���漰��ѧ֪ʶ�����������������
A��������������첣����Ҳ�����ڳ�ȥ��Ʒ���������
B���þ�����ϩ����ľ��������װ�С���ͺеȣ��Լ���ľ�ĵ�ʹ��
C���ƺ��˺���ɳ���γɺ�±ˮ�㶹�����������˽���۳�������
D����ú����������ú�ĵ�����ȼ�ϸ��칤�������ڼ��ٻ�����Ⱦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ԭ�Ӿ�����������ṹ���ǣ� ��
A. CH4 B. CH3Cl C. C2H6 D. C2H4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����칬���š���2016��9��15�շ���ɹ������ҹ��Ƽ���չ�ļ������֡�������Դ�Ͳ��ϣ�����˵���������
A�����ά����Ϣ��ҵ���й㷺��Ӧ�ã�������ά����Ҫ�����Ƕ�������
B��ú�ĸ���������Һ�������ڻ�ѧ�仯
C����������������Դʱ�������ܡ�̫���ܺ����ܵȺܿ��ܳ�Ϊ��Ҫ��Դ
D�����ϲ��������л����Ӳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A. ������������ɢϵ�ı��������Ƿ�ɢ������ֱ���Ĵ�С��1-100 nm֮��
B. �������ö����ЧӦ���ֽ������Һ
C. ������ܷ��������˶��͵�Ӿ����
D. ������һ�����������ȶ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ����þ��MgSO47H2O����ӡȾ����ֽ��ҽҩ�ȹ�ҵ�϶��й㷺��Ӧ�ã����û�����������ɰ�ķ�������þ�����ȡ��ˮ����þ����þ�����Ҫ�ɷ���MgCO3���������������ʣ�MgO��SiO2��Fe2O3��FeO��CaO��Al2O3��MnO�ȣ���
��1 ����������������������ʽ��ȫ����ʱ��Һ��pH
������ | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Mn��OH��2 | Mg��OH��2 | ||||||
pHֵ | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 | ||||||
��2 �����ε��ܽ�ȣ���λΪg/100gˮ��
�¶�/�� | 10 | 30 | 40 | 50 | 60 | ||||||||||||
CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 | ||||||||||||
MgSO47H2O | 30.9 | 35.5 | 40.8 | 45.6 | / | ||||||||||||
��þ����ȡ��ˮ����þ�Ĺ����������£�
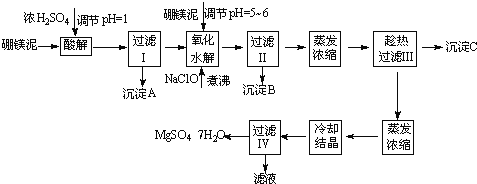
������������ͼ���ο�����pH���ݺ��ܽ�����ݣ��Իش��������⣺
��1������I����Һ�м�����þ�࣬������Һ��pH=5��6���ټ���NaClO��Һ������У�����Һ�е�Mn2+������MnO2����Ӧ�����ӷ�Ӧ����ʽΪ ��������е���ҪĿ���� ��
��2������B�г�MnO2��SiO2����� ���ѧʽ����������
��3��������ˢ�����Һ���Ƿ���Fe3+��ʵ�鷽���� ��
��4������C�Ļ�ѧʽ�� �����ˢ�����ȹ��˵������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ���ǣ� ��
A��NH3��Һ���������������
B��NH4Cl�к���������I2��ͨ�����ȵķ�����ȥ
C����������ֽ⣬������氱̬����ʱҪ�ܷⱣ�棬����������ͨ�紦
D��Ũ�����豣������ɫƿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯������������������������Ҫ����;����֪��Sn���۵�Ϊ231����Sn2+��ˮ�⡢�ױ�������SnCl4����ˮ�⡢�۵�Ϊ-33 �����е�Ϊ114 �����밴Ҫ��ش�����������⣺
��1��Ԫ������ͬ����̼����������3������ԭ������Ϊ_______________��
��2�����������������������۴��Ȳⶨ����ȡ1.19 g��������ϡ�����У����ʲ����뷴Ӧ����ʹSn��ȫת��ΪSn2+�������������Fe2(SO4)3������0.1000 mol/L K2Cr2O7��Һ�ζ���������Cr��+3�ۣ�������20.00 mL���������м���Fe2(SO4)3��������__________________����������Ʒ��������������_____________��
��3�����ڶ�����ҵ����������(SnSO4)���Ʊ�·�����£�
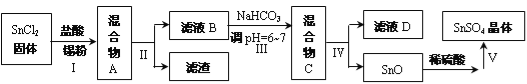
������������Sn�۵����ã� __________________��������ҺpH��
�����������������IJ�������Ϊ________________��д���ù����õ���һ�ֲ������������ƣ�_______________��
������������SnO�����ӷ���ʽ��__________________��
����������������Ϊ _____________��____________�����ˡ�ϴ�ӡ����¸��
��4��SnCl4����������ˮ����Ũ��״�������������Ļ�����䷴Ӧ�Ļ�ѧ����ʽΪ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������þӦ�ù㷺������þ��(��Ҫ�ɷ�ΪMgCO3��SiO2��FeCO3)Ϊԭ���Ʊ��ߴ�����þ��ʵ���������£�
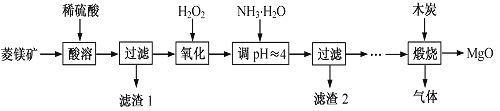
��1��MgCO3��ϡ���ᷴӦ�����ӷ���ʽΪ ��
��2������H2O2ʱ����Ӧ�����ӷ���ʽΪ ��
��3������1������2�ijɷֱַ��� (�ѧʽ) �� ��
��4�����չ��̴������·�Ӧ��
2MgSO4+C![]() 2MgO+2SO2��+CO2��
2MgO+2SO2��+CO2��
MgSO4+3C![]() MgO+S��+3CO��
MgO+S��+3CO��
���������չ����в�����SO2����ˮ���գ����ӷ���ʽΪ__________________
���õ��ĵ���ɫ����S���ȵ�NaOH��Һ��Ӧ��������Ԫ�����̬Ϊ+4��д���÷�Ӧ�����ӷ���ʽ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com