
| A、57 | B、47 | C、64 | D、293 |
科目:高中化学 来源: 题型:
| A、该反应是放热反应,降低温度将缩短反应达到平衡的时间 |
| B、恒温恒容下往平衡体系通入氩气,反应体系的压强会增大,反应速率也必定增大 |
| C、恒温恒压下往平衡体系通入氩气,反应体系的体积会增大,平衡体系朝逆向移动 |
| D、合成氨的适宜条件是高温、高压、催化剂,其中催化剂不改变该反应的逆反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、9种 | B、12种 |
| C、15种 | D、18种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓硝酸与浓盐酸一样,在空气中出现白雾 |
| B、硝酸见光分解和受热分解产物相同,都是NO2、O2和H2O |
| C、NO2与水反应有硝酸生成,所以NO2是硝酸酸酐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、体系压强不再发生变化 |
| B、各组分的物质的量浓度不再改变 |
| C、各组分的质量分数不再改变 |
| D、反应速率vA:vB:vC:vD=m:m:p:q |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 | 实验内容 | 实验目的 |
| A | 将木炭与浓硫酸共热,得到的气体通入澄清石灰水 | 检验木炭的氧化产物是CO2 |
| B | 加入足量铁屑,充分反应后,过滤 | 除去FeCl2溶液中的少量FeCl3 |
| C | 将1molCuSO4?5H2O溶解在1L 水中 | 制备1moL/L的CuSO4溶液 |
| D | 饱和氯化铁溶液中滴加氨水 | 制备Fe(OH)3胶体 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
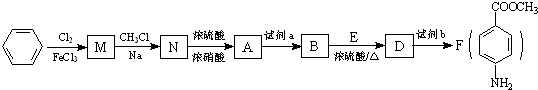
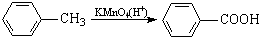


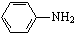 最多能够和
最多能够和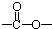 结构;
结构;查看答案和解析>>
科目:高中化学 来源: 题型:
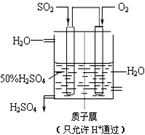 工业上生产硫酸时,将SO2氧化为SO3是关键一步.
工业上生产硫酸时,将SO2氧化为SO3是关键一步.| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com