
分析 (1)根据配制一定物质的量浓度的溶液的操作步骤选择使用的仪器;
(2)根据稀释定律C浓V浓=C稀V稀来计算并根据需要的浓硫酸的体积来选择合适的量筒;
(3)根据配制步骤判断玻璃棒的作用;
(4)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(5)根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
(6)根据方程式计算参加反应的锌、硫酸的物质的量;根据m=nM计算锌的质量,溶液中n(H+)=2n(H2SO4),计算出硫酸的物质的量浓度变化量,即可求出氢离子浓度变化量,氢离子开始浓度减去氢离子浓度变化量等于反应后溶液中的氢离子的物质的量浓度.
解答 解:(1)配制溶液的操作步骤:首先计算出需要的药品的体积,然后用量筒量取,后放入烧杯中稀释,同时用玻璃棒搅拌,待溶液冷却至室温后,用玻璃杯引流移液至500ml容量瓶,然后洗涤烧杯和玻璃棒2至3次,将洗涤液也注入容量瓶,然后向容量瓶中注水,至液面离刻度线1至2CM时,改用胶头滴管逐滴加入,至凹液面与刻度线相切,然后摇匀、装瓶.用到的仪器有:量筒、烧杯、玻璃棒、500ml容量瓶、胶头滴管.故不需要的有:④⑤,还缺少的一种主要仪器是:500ml容量瓶.故答案为:④⑤;500ml容量瓶;
(2)设需要的浓硫酸的体积为VmL,根据稀释定律C浓V浓=C稀V稀可知:18.4mol/L×Vml=500mL×0.2mol/L
解得V=5.4mL.根据容量瓶的选用规则是“大而近”,故选用10ml的量筒.故答案为:5.4;
(3)实验中两次用到玻璃棒,溶解氢氧化钠溶液时需要使用玻璃棒搅拌、转移溶液时用玻璃棒引流,故答案为:搅拌,引流;
(4)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知操作顺序为:②→①→③→⑧→⑤→⑥→⑦→④,故答案为:⑧→⑤→⑥→⑦;
(5)①定容时,仰视刻度线,会导致溶液体积偏大,则浓度偏低,故正确;
②未冷却至室温就转移到容量瓶中,待冷却后溶液体积偏小,故浓度偏高,故错误;
③容量瓶中含有少量蒸馏水,对浓度无影响,故错误;
④未洗涤稀释浓硫酸时用过的烧杯和玻璃棒,则会导致溶质的损失,浓度偏低,故正确;
⑤定容摇匀后,发现液面低于刻度线是正常的,又用胶头滴管加蒸馏水至刻度线,则浓度偏低,故正确.
故选①④⑤;
(6)Zn+H2SO4 =ZnSO4 +H2↑
1mol 1mol 22.4L
x y 0.224L
所以x=$\frac{0.224L}{22.4L/mol}$=0.01mol.
y=x=0.01mol.
所以参加反应锌的质量为0.01mol×65g/mol=0.65g.
氢离子浓度变化量为△c(H+)=$\frac{0.02mol}{0.1L}$=0.2mol/L.
所以反应后溶液中的氢离子的物质的量浓度为0.4mol/L-0.2mol/L=0.2mol/L.
故答案为:2.6g;0.2mol/L.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算、误差分析和根据化学方程式来计算,属于基础型题目,难度不大.


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 5.4 g | B. | 8.4 g | C. | 4.1g | D. | 9.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 试剂 温度 | T1/℃ | T2/℃ | T3/℃ |
| Na2CO3 | 23.3 | 20.0 | 23.7 |
| NaHCO3 | 18.5 | 20.0 | 20.8 |
温度 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 40.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaX的水溶液的碱性一定强于NaY水溶液的碱性 | |
| B. | HX一定是弱酸 | |
| C. | 反应结束时两者所用时间相同 | |
| D. | 浓度:C(HX)>C(HY) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
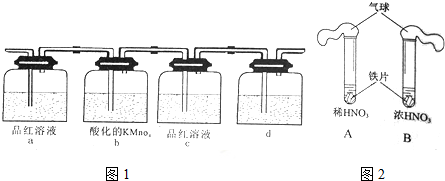
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在加热条件下能使不活泼金属铜溶解,表现出浓硫酸的强氧化性和酸性 | |
| B. | 可以用铁制或铝制容器贮运,表现出浓硫酸有稳定的化学性质 | |
| C. | 能使胆矾晶体由蓝色变为白色,表现出浓硫酸的脱水性 | |
| D. | 能使蔗糖炭化,表现出浓硫酸的吸水性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com