
【题目】以工业制立德粉后的铅锌废渣(主要成分为ZnO和PbSO4,杂质含Si、Fe、Cu、Cd等元素)为原料,可以制活性氧化锌和黄色颜料铅铬黄,工业流程如图所示:

已知:Ksp(PbSO4)=1.6×10-8,Ksp(PbCO3)= 7.4×10-14
(1)“碱浸”过程中PbSO4发生反应的离子方程式为_________________________,气体A 的化学式为____________________。
(2)“酸浸”过程中pH不宜过低,若pH过低,可能出现的问题是___________________________。
(3)“沉降I”过程中发生反应的离子方程式为_____________________________________。
(4)滤液D中溶质的主要成分为_____________,为制得较为纯净的ZnO,“煅烧”之前应该进行的操作I是_____________________________。
(5)以1t含锌元素10%的铅锌废渣为原料,制得活性氧化锌113.4kg,依据以上数据_______(填“能”或“不能”)计算出锌元素的回收率。若能,写出计算结果,若不能,请说明理由________________________________________________。
【答案】 PbSO4 (s) + CO32─(aq) ![]() PbCO3(s) + SO42─ (aq) CO2 铁元素以离子形式进入到滤液C中,影响PbCrO4纯度 2Pb2++ 2OH─+Cr2O72─=2PbCrO4↓+H2O (NH4)2SO4 洗涤、干燥 不能 除去铜、镉的过程中添加了锌粉,最终ZnO中的锌元素不完全来自于铅锌废渣,无法计算铅锌废渣中锌元素的回收率
PbCO3(s) + SO42─ (aq) CO2 铁元素以离子形式进入到滤液C中,影响PbCrO4纯度 2Pb2++ 2OH─+Cr2O72─=2PbCrO4↓+H2O (NH4)2SO4 洗涤、干燥 不能 除去铜、镉的过程中添加了锌粉,最终ZnO中的锌元素不完全来自于铅锌废渣,无法计算铅锌废渣中锌元素的回收率
【解析】(1)已知Ksp(PbSO4)=1.6×10-8>Ksp(PbCO3)= 7.4×10-14.所以 “碱浸”过程中PbSO4发生反应的离子方程式为 PbSO4 (s) + CO32─(aq) ![]() PbCO3(s) + SO42─ (aq),固体A为PbCO3(s)
PbCO3(s) + SO42─ (aq),固体A为PbCO3(s)
酸浸后产生的气体为CO2, A 的化学式为CO2。答案:PbSO4 (s) + CO32─(aq) ![]() PbCO3(s) + SO42─ (aq) CO2
PbCO3(s) + SO42─ (aq) CO2
(2)“酸浸”过程中pH不宜过低,若pH过低,酸性强,使Fe与酸反应生成有关铁的化合物,进入到滤液C中,再加碱进行沉降时,会出现Fe(OH)3沉淀,影响PbCrO4纯度。答案:铁元素以离子形式进入到滤液C中,影响PbCrO4纯度。
(3)由 知“沉降I”过程中发生反应的离子方程式为. 2Pb2++2OH─+Cr2O72─=2PbCrO4↓+H2OO
知“沉降I”过程中发生反应的离子方程式为. 2Pb2++2OH─+Cr2O72─=2PbCrO4↓+H2OO
(4)由图知滤液B中含有的离子为Zn2- NH4+ CO32─ ,加H2SO4调节溶液的PH=6-6.5出现![]() 沉淀,滤液为(NH4)2SO4,所以滤液D中溶质的主要成分为(NH4)2SO4。
沉淀,滤液为(NH4)2SO4,所以滤液D中溶质的主要成分为(NH4)2SO4。
为制得较为纯净的ZnO,“煅烧”之前应该对固体进行洗涤干燥处理。答案:(NH4)2SO4 洗涤、干燥。
(5)根据图知不能,因为在除去铜、镉的过程中添加了锌粉,最终ZnO中的锌元素不完全来自于铅锌废渣,无法计算铅锌废渣中锌元素的回收率。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】磷酸铁锂动力电池(LiFePO4电池)是一种新型动力电池。电池的内部结构如图所示。中间是聚合物的隔膜,它把正极与负极隔开,Li+可以通过而e-不能通过。该电池的总反应式为:Li1-xFePO4+LixC6![]() C6 +LiFePO4 (注:LixC6是单质Li附在碳电极上的一种形式)。下列关于该电池的叙述错误的是
C6 +LiFePO4 (注:LixC6是单质Li附在碳电极上的一种形式)。下列关于该电池的叙述错误的是

A. 放电时, LixC6在负极上失电子发生氧化反应
B. 在充电时,正极中的Li+通过聚合物隔膜向负极迁移
C. 放电时,正极反应式为Li1-xFePO4+xLi+= LiFePO4-xe-
D. 若用该电池电解精炼铜,阴极质量增重19.2kg时,则电池中通过聚合物隔膜的Li+数目为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】充分燃烧2.8g某有机物A,生成8.8g CO2和3.6g H2O,这种有机物蒸气的相对密度是相同条件下N2的2倍.
(1)该有机物的分子式为 .
(2)该有机物链状同分异构体的结构简式为 .
(3)若在核磁共振氢谱中只有一个信号峰(即只有一种氢原子),则用键线式表示的结构简式为 . 该分子的所有碳原子能否在一个平面上(填“能”或“不能”) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关细胞分子的叙述,正确的是( )
A. 携带遗传信息是核酸的唯一功能
B. 叶肉细胞中缺乏 Mg 元素,则影响叶绿素合成
C. 氨基酸的空间结构是蛋白质多样性的原因
D. 等质量脂肪氧化分解比糖释放能量多是因为脂肪分子中氧含量多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列各组微粒或物质:
A、O2和O3
B、 ![]() 和
和 ![]()
C、CH3CH2CH2CH3和 ![]()
D、 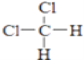 和
和 
E、CH3CH2CH2CH3和 ![]()
(1)________组两种微粒互为同位素;
(2)________组两种物质互为同素异形体;
(3)________组两种物质属于烃;
(4)________组两物质互为同分异构体;
(5)________组两物质是同一物质.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铝片与1molL-1稀盐酸反应制取氢气时,下列措施不能使氢气生成速率增大的是
A.对该反应体系加热B.用浓硫酸代替稀盐酸
C.加入少量硫酸铜溶液D.加入少量1molL-1硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下图所示化合物的说法不正确的是 ( ) 
A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1mol该化合物最多可以与3molNaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学假说是科学发展的一种重要形式。有科学家提出: 利用空气中的二氧化碳与氢气反应后,使之变为可再生的燃料甲醇的设想。其设想的生产流程如图。下列说法正确的是

A. 上述流程中饱和碳酸钾溶液所起的作用是降低空气中的CO2 的溶解度
B. 上述流程中能体现“循环利用”的物质有碳酸氢钾溶液和高温水蒸气
C. 从合成塔中分离出甲醇的实验操作方法是分液
D. 通入高温水蒸气的作用是: 加快CO2的生成和逸出,以便及时提供给合成塔
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com