
 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:可能用到的有关数据如下:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:可能用到的有关数据如下:| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
分析 在a中加入20g环己醇和2小片碎瓷片,碎瓷片能防暴沸,冷却搅动下慢慢加入1mL浓硫酸,相当于浓硫酸的稀释,不能将环己醇倒入浓硫酸中;b中通入冷却水后,开始缓慢加热a,在浓硫酸作催化剂条件下,环己醇发生消去反应生成环己烯,根据二者沸点知,要想得到较纯净的环己烯,应该控制馏出物的温度不超过90℃;反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,氯化钙作干燥剂,然后静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g,
(1)装置b的名称是冷凝管;
(2)碎瓷片有放暴沸作用;补加碎瓷片时需要待已加热的试液冷却后再加入;
(3)分液漏斗在使用前须清洗干净并检漏;分液过程中,由于环己烯的密度比水的密度小,故应该从分液漏斗的上口倒出;
(4)无水氯化钙能作干燥剂;
(5)在环己烯粗产物蒸馏过程中,根据各仪器的作用选取仪器;
(6)环己醇的物质的量=$\frac{20g}{100g/mol}$=0.2mol,根据C原子守恒知,理论上生成环己烯的物质的量也是0.2mol,其质量=0.2mol×82g/mol=16.4g,生成的本实验所得到的环己烯产率=$\frac{10g}{16.4g}×100%$.
解答 解:在a中加入20g环己醇和2小片碎瓷片,碎瓷片能防暴沸,冷却搅动下慢慢加入1mL浓硫酸,相当于浓硫酸的稀释,不能将环己醇倒入浓硫酸中;b中通入冷却水后,开始缓慢加热a,在浓硫酸作催化剂条件下,环己醇发生消去反应生成环己烯,根据二者沸点知,要想得到较纯净的环己烯,应该控制馏出物的温度不超过90℃;反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,氯化钙作干燥剂,然后静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g,
(1)装置b的名称是冷凝管,故答案为:冷凝管;
(2)碎瓷片的存在可以防止在加热过程中产生暴沸现象,补加碎瓷片时需要待已加热的试液冷却后再加入,故选D,
故答案为:防止暴沸;D;
(3)由于分液漏斗有活塞开关,故使用前需要检查是否漏液;分液过程中,由于环己烯的密度比水的密度小,故应该从分液漏斗的上口倒出,
故答案为:检漏;上口倒出;
(4)分离提纯过程中加入无水氯化钙的目的是利用无水氯化钙吸收产物中少量的水,
故答案为:干燥;
(5)观察题目提供的实验装置图知蒸馏过程中不可能用到吸滤瓶和球形冷凝器管,
故选:C;
(6)环己醇的物质的量=$\frac{20g}{100g/mol}$=0.2mol,根据C原子守恒知,理论上生成环己烯的物质的量也是0.2mol,其质量=0.2mol×82g/mol=16.4g,生成的本实验所得到的环己烯产率=$\frac{10g}{16.4g}×100%$=61%,
故选C.
点评 本题考查制备实验方案设计,为高频考点,明确实验原理及实验操作顺序是解本题关键,注意从实验安全性、评价性、操作规范性等方面分析解答,充分利用题给信息解答问题,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 10 mL 0.1 mol•L-1的氯化铝溶液 | B. | 20 mL 0.1 mol•L-1的氯化钙溶液 | ||
| C. | 30 mL 0.2 mol•L-1的氯化钾溶液 | D. | 40 mL 0.25 mol•L-1的氯化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 1 mol荧火黄完全燃烧消耗标准状况下氧气体积为459.2L | |
| B. | 荧火黄分子中含有两种含氧官能团 | |
| C. | 1 mol荧火黄最多可与含4 mol NaOH的溶液完全反应 | |
| D. | 荧火黄的分子式为C20H14O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
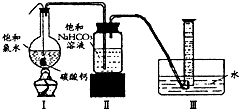 饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.某《化学教育》杂志报道了如下实验研究:
饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.某《化学教育》杂志报道了如下实验研究:查看答案和解析>>
科目:高中化学 来源: 题型:填空题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应N2+3H2?2NH3的平衡常数K值和温度的关系如下:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应N2+3H2?2NH3的平衡常数K值和温度的关系如下:| 温度/℃ | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com